АКТУАЛЬНОСТЬ
Внебольничная пневмония (ВП) является наиболее распространенным острым инфекционным заболеванием с высокой смертностью [1]. В России заболеваемость ВП в 2021 г. была на уровне 1366,6 случаев на 100 тыс. всего населения (1 997 536 человек) [2]. Частота госпитализации при ВП многократно возрастает среди лиц с факторами риска [3].
Сахарный диабет – один из наиболее значимых факторов риска развития и тяжелого течения ВП среди взрослого населения из числа хронических заболеваний [4, 5]. Согласно данным Федерального регистра сахарного диабета РФ по состоянию на начало 2021 г., количество больных СД составило в нашей стране 4 799 552 человека (3,23% населения), включая 4,43 млн (92,5%) пациентов с СД 2-го типа (СД 2). При этом наблюдается быстрый рост числа новых случаев диабета [6].
Пневмонии у пациентов с СД отличаются более высоким риском развития осложнений, они склонны к затяжному течению и часто сопровождаются выраженной и длительной декомпенсацией коморбидной патологии [7, 8].
Клинические исходы ВП среди пациентов с СД 2 зависят от различных факторов, выявление которых позволит предотвратить развитие неблагоприятных последствий и оптимизировать процесс терапии. Такие факторы риска служат основой для разработки системы поддержки принятия врачебных решений, позволяющих врачу на основе индивидуальных клинико-лабораторных и других данных о пациенте выстроить правильную тактику ведения больного.
В настоящее время недостаточно изученным остается вопрос о том, какие клинико-лабораторные маркеры и их ассоциации снижают вероятность эффективности стартовой эмпирической антибактериальной терапии (АБТ) ВП среди пациентов с СД 2, увеличивают вероятность развития острых диабетических и недиабетических осложнений.
Цель исследования – установить факторы, ассоциированные с неэффективностью стартовой эмпирической АБТ, а также с развитием острых диабетических и недиабетических осложнений в процессе терапии ВП среди госпитализированных пациентов с СД 2.
МАТЕРИАЛ И МЕТОДЫ
По дизайну исследование было проспективным интервенционным одноцентровым. В нем приняли участие 54 пациента с ВП, ассоциированной с СД 2, госпитализированных в пульмонологическое отделение ГБУ «Республиканская клиническая больница имени Ш.Ш. Эпендиева» (г. Грозный) в период с 01.01. по 01.07.2019.
Критерии включения: наличие диагноза ВП; возраст 18 лет и старше; информированное согласие пациента.
Критерии исключения: возраст до 18 лет и выше 89 лет; СД 1-го типа; отказ пациента от участия в исследовании.
Диагноз ВП подтверждался в соответствии с критериями, указанными в клинических рекомендациях по лечению этого заболевания [9]. Тяжесть ВП определялась с использованием критериев IDSA/ATS. Диагноз СД 2 основывался на анамнестических данных, подтвержденных медицинской документацией, либо учитывался в случае, если пациенту было назначено лечение пероральными сахароснижающими препаратами (ПССП) или инсулином. Наличие осложнений СД 2 определялось в соответствии «Алгоритмом специализированной медицинской помощи больным сахарным диабетом [10]. Стартовая этиотропная АБТ назначалась согласно клиническим рекомендациям по лечению ВП с учетом факторов риска, аллергических реакций на АБП, сопутствующих болезней [9].
Всем больным ВП, ассоциированной с СД 2, при поступлении назначались препараты инсулина в соответствии с Алгоритмами специализированной медицинской помощи больным СД [10]. Дозу инсулина подбирали так, чтобы достичь индивидуальных целевых показателей гликемического контроля.
До назначения системных АБП у пациентов собирались образцы свободно отделяемой или при необходимости индуцированной мокроты, перед началом искусственной вентиляции легких (ИВЛ) – трахеальный аспират. При тяжелой ВП отбирались два образца венозной крови из разных периферических вен. Собранные образцы направлялись в локальную лабораторию для культурального исследования.
Статистический анализ данных: количественные признаки, соответствующие нормальному распределению, представлены в виде среднего значения (М) и стандартного отклонения (SD), 25%-ного и 75%-ного квартилей, качественные признаки – в виде абсолютных чисел и долей. Расчет показателей отношения шансов (ОШ) для бинарного признака проводился при помощи построения четырехпольных таблиц сопряженности с расчетом критерия χ2 Пирсона. В случае невыполнения условия применимости критерия χ2 Пирсона (независимость групп, более 25% ячеек в четырехпольной таблице сопряженности имеют ожидаемую частоту менее 5), выполнялся расчет критерия Фишера (2р(F)). Для количественного признака (возраст) ОШ рассчитывалось посредством логистического регрессионного анализа. Статистический анализ производился с использованием программы IBM SPSS Statistics 23.0.
Исследование было одобрено Локальным этическим комитетом Медицинского института ФГАОУ ВО «Российский университет дружбы народов» (протокол от 17.06.2021 г. № 30).
РЕЗУЛЬТАТЫ
Клинико-демографические и анамнестические характеристики исследованных больных ВП, ассоциированной с СД 2, приведены в таблице 1.
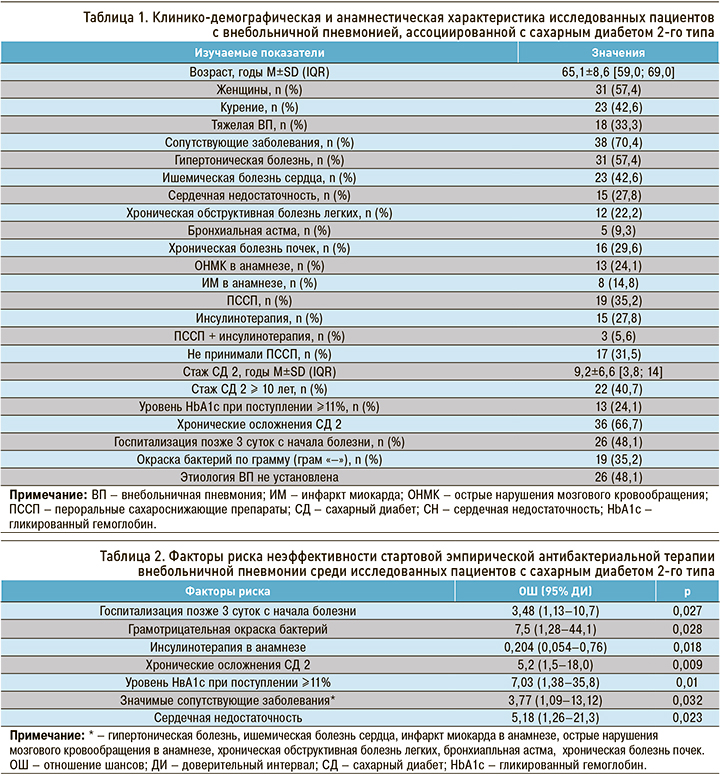
Среди пациентов с СД 2 эффективная стартовая эмпирическая АБТ ВП наблюдалась в 46,3% (25/54) случаев, неэффективная – в 53,7% (29/54). Отсутствие эффективности стартовой эмпирической АБТ было ассоциировано с госпитализацией позже третьих суток от начала болезни, грамотрицательной бактериальной флорой, наличием хронических осложнений СД 2, уровнем гликированного гемоглобина при поступлении ≥11%, наличием значимых сопутствующих заболеваний, в том числе сердечной недостаточности (табл. 2).
Отметим, что инсулинотерапия в анамнезе, в отличие от других перечисленных факторов риска, увеличивает вероятность успешной эмпирической АБТ ВП на 79,6%.
Среди пациентов с СД 2 острые недиабетические осложнения в процессе терапии ВП развились в 29,6% (16/54) случаев, лечение прошло без осложнений у 70,4% (38/54) больных. Установлены факторы риска, ассоциированные с развитием острых недиабетических осложнений в процессе терапии ВП у пациентов с СД 2. Так, у пациентов с СД 2, госпитализированных с тяжелой ВП, риск развития недиабетических осложнений в процессе лечения в 6 раз выше, по сравнению с больными СД 2, госпитализированными с нетяжелой ВП. При наличии ХОБЛ риск развития осложнений возрастает в 5 раз, при ОНМК в анамнезе – в 4,2 раза, при отсутствии эффекта от стартовой эмпирической АБТ ВП – в 6 раз, при уровне гликированного гемоглобина на этапе поступления ≥11 % – в 4,2 раза. С каждым годом стажа СД 2 риск развития недиабетических осложнений возрастает в 1,097 раза или на 9,7% (табл. 3).
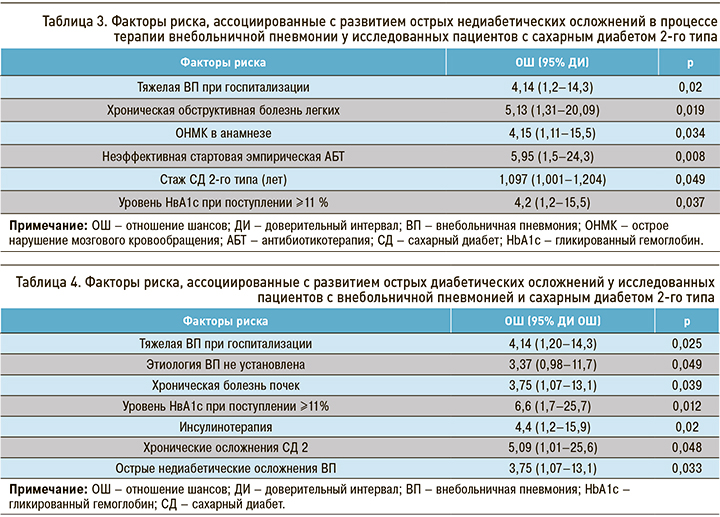
Острые диабетические осложнения в процессе терапии ВП возникли в 29,6% случаев (16/54). К факторам, ассоциированным с высоким риском развития таких осложнений в процессе лечения ВП, относятся тяжелая ВП при поступлении в стационар, неизвестная этиология ВП после микробиологических исследований, наличие хронической болезни почек (ХБП), уровень гликированного гемоглобина при поступлении ≥11%, а также наличие острых недиабетических и хронических диабетических осложнений (табл. 4).
При этом у пациентов с ВП и СД 2 между острыми недиабетическими осложнениями ВП и острыми диабетическими осложнениями имеется статистически значимая прямая зависимость (rСпирмена = 0,289, р =0,034).
ОБСУЖДЕНИЕ
Актуальность повышения эффективности стартовой эмпирической АБТ определяется высокой распространенностью и социальной значимостью ВП среди пациентов с СД 2. Несмотря на достаточно широкий имеющийся арсенал различных групп антимикробных препаратов, используемых для лечения ВП, среди пациентов с СД 2 эффективность АБТ остается на низком уровне. Недостаточная эффективность рутинных методов этиологической диагностики ВП, составляющей 24–50% случаев [11–13], затрудняет эффективное этиотропное лечение, которое будет оставаться эмпирическим до разработки точных и доступных тестов. В связи с этим врачи должны быть осведомлены не только о спектре микроорганизмов, циркулирующих на их территории [14], но и факторах риска, ассоциированных с неэффективностью эмпирической АБТ при ВП.
В результате проведенного нами анализа установлены факторы, ассоциированные с повышенной вероятностью неэффективной стартовой эмпирической АБТ ВП среди госпитализированных пациентов с СД 2. К ним относятся поздняя госпитализация, грамотрицательная бактериальная флора, сопутствующие хронические заболевания, хронические осложнения СД, уровень гликированного гемоглобина при поступлении ≥11%.
Полностью аналогичных нашему исследований, в которых бы изучались факторы риска неэффективности стартовой АБИ ВП, не проводилось. Тем не менее в исследовании Yende S. et. al. (2010) показано, что при ВП грамотрицательные микроорганизмы чаще встречались среди пациентов с СД, а грамположительные – среди лиц без СД (7,5 и 3,1% соответственно; p=0,001) [15]. В другом исследовании грамотрицательная флора при ВП у лиц с СД также выявлялась с более высокой частотой (10,5 против 1,9% у лиц без СД; р=0,01), при этом она была ассоциирована с повышенной летальностью (ОШ=5,7; 95% ДИ: 1,28–25,12; р=0,02) [16]. Косвенным подтверждением более низкой эффективности проводимого лечения ВП среди пациентов с СД может служить длительность госпитализации, которая, по данным исследования Martins M. et. al. (2016), выше у больных с СД, по сравнению с лицами без СД (12,0±10,5 и 11,2±10,1 соответственно; р <0,0001); кроме того, при наличии СД выше госпитальная летальность (15,2 против 13,5%; р= 0,002) [17].
Аналогичные данные представлены Huang D. et. al. (2021), которые установили, что у больных с тяжелой ВП и СД 2 имели место бόльшая продолжительность нахождения в ОРИТ (13 против 12 дней; р=0,016), более высокие госпитальная смертность (35,2 против 31,0%; р=0,009) и 14-дневная смертность (15 против 10,8%, p <0,001) по сравнению с пациентами без СД 2 [18].
Выявленные факторы позволят специалистам выделить больных ВП, ассоциированной с СД 2, в отношении которых есть повышенная вероятность неэффективной стартовой эмпирической АБТ.
Инфекции, зачастую осложняющие течение СД и приводящие к его декомпенсации (пневмония среди них встречается с частотой от 38,7 до 40,9%), являются наиболее частыми провоцирующими факторами развития острых диабетических осложнений, частота которых достигает более 70,0% [19, 20].
В нашем исследовании среди пациентов с СД 2 острые диабетические осложнения, так же как и недиабетические, развивались в процессе терапии ВП в 1/3 случаев. К факторам, ассоциированным с развитием острых недиабетических осложнений, относятся тяжесть ВП, хроническая обструктивная болезнь легких, острые нарушения мозгового кровообращения в анамнезе, отсутствие эффекта от стартовой эмпирической АБТ ВП, уровень гликированного гемоглобина при поступлении ≥11 %, а также стаж СД 2. С развитием острых диабетических осложнений ассоциированы тяжелая ВП, неизвестная ее этиология, ХБП, уровень гликированного гемоглобина при поступлении ≥11%, инсулинотерапия в анамнезе, острые недиабетические и хронические диабетические осложнения. Выявленные нами факторы риска неблагоприятного клинического исхода ВП среди пациентов с СД 2 в своем большинстве согласуются с результатами других исследований.
Данные исследования Di Yacovo S. et. al. (2013) также показали, что у 516 больных СД во время госпитализации, связанной с ВП, часто отмечались острые метаболические нарушения, такие как гипергликемия (5,8%), диабетический кетоацидоз (2,5%). Помимо этого, авторы установили более высокую частоту развития септического шока у пациентов с СД, в отличие от пациентов без СД (28,9 и 7,7% соответственно, р <0,001) [16].
Zeng W. et. al. (2022) установили, что среди пациентов с СД ХБП и уровень гликемии при поступлении >11,1 ммоль/л выступают факторами риска, связанными с высокой частотой госпитализации в ОРИТ (ОШ=3,85; 95% ДИ 2,15–6,89; р <0,001 и ОШ=3,02; 95% ДИ 1,31–6,99; р =0,010 соответственно) [21]. В другом исследовании показано, что возрастание количества сопутствующих заболеваний (р <0,001) и хронических диабетических осложнений (р <0,001) увеличивают вероятность смерти пациентов с ВП, ассоциированной с СД 2 [18].
Согласно данным Zhang L. et. al. (2022), степень повышения лактата артериальной крови и соотношение лактата к альбумину сыворотки (Lac/Alb) прямо коррелировали с повреждением миокарда у пожилых пациентов с тяжелой ВП, среди которых уровень смертности в ОРИТ был значительно выше, чем в группе без повреждения миокарда (72,0 против 36,2%, p <0,01) [22]. При этом известно, что гипоксия при ВП может спровоцировать развитие лактатацидоза, особенно у пациентов с относительной инсулиновой недостаточностью.
Таким образом, проведенное нами исследование позволило установить факторы, ассоциированные с неблагоприятными клиническими исходами ВП среди госпитализированных пациентов с СД 2, которые могут быть использованы врачом для выработки правильной тактики ведения таких больных в условиях стационара.
ЗАКЛЮЧЕНИЕ
В результате проведенного исследования установлены факторы, ассоциированные с неэффективностью стартовой эмпирической АБТ, с развитием острых диабетических и недиабетических осложнений в процессе терапии ВП среди госпитализированных пациентов с СД 2. Практикующие врачи должны сосредоточить внимание не только на лечение ВП, но и на выявление факторов, ассоциированных с развитием неблагоприятных клинических событий среди госпитализированных пациентов с СД 2, поскольку они значимо сказываются на эффективности терапии, а также на частоте развития острых диабетических и недиабетических осложнений, влияющих на исход основного заболевания.



