Некомпактный миокард желудочков – форма кардиомиопатии, характеризующаяся патологической трабекулярностью миокарда. Достоверные статистические данные о его распространенности отсутствуют [1].
Некомпактный миокард обычно изолированно поражает левый желудочек (ЛЖ), реже встречается бивентрикулярное поражение [1, 2]. Описаны единичные случаи изолированной формы некомпактного миокарда правого желудочка (НМПЖ) [3–8]. Вопрос об изолированной форме НМПЖ является дискутабельным, так как трудно отличить нормальный и патологический варианты повышенной трабекулярности ПЖ [3]. Кроме того, повышение трабекулярности наблюдается при аритмогенной дисплазии правого желудочка (АДПЖ) [9]. Изолированный НМПЖ до настоящего время не имеет четкого стандарта диагностики [3].
Ниже приводится клинический случай диагностики у 40-летнего пациента изолированного НМПЖ, осложненного тромбоэмболией легочной артерии (ТЭЛА).
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ
Пациент Н., 40 лет, поступил в ЛПУ с жалобами на общую слабость, учащенное сердцебиение и одышку в покое, усиливающиеся при незначительной физической нагрузке, немотивированную потливость, редкий непродуктивный кашель. Указанные жалобы появились и стали прогрессировать за 2 нед до обращения, длительно отмечалась низкая толерантность к физической нагрузке. При осмотре отмечались одышка инспираторного типа с частотой до 30 в минуту, тахиаритмия 116 уд./мин, пульс слабого напряжения, артериальное давление (АД) 110/80 мм рт. ст., SpO2 78%.
Холтеровское мониторирование электрокардиограммы (ЭКГ) выявило у пациента нарушения сердечного ритма (рис. 1).
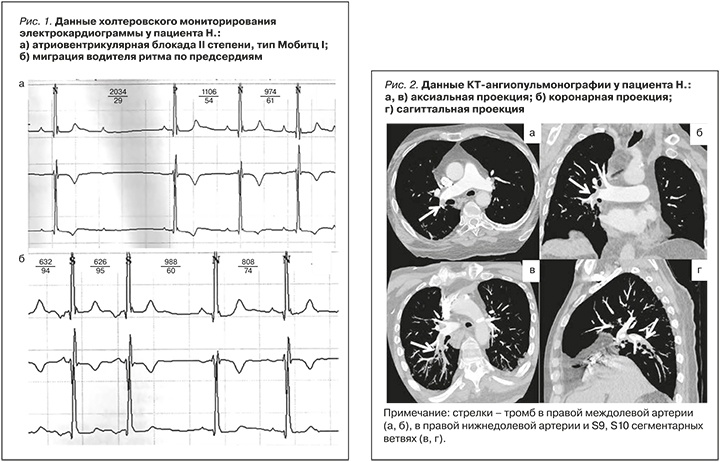
По данным эхокардиографии (ЭхоКГ) наблюдались дилатация правых камер сердца, ствола и ветвей легочной артерии, трикуспидальная регургитация 3 ст., утолщение стенки ПЖ и парадоксальное движение межжелудочковой перегородки. Выявлена легочная гипертензия со значением среднего давления в легочной артерии (СДЛА) 86 мм рт.ст. (норма СДЛА составляет ≤20 мм рт. ст.).
При обследовании отмечалось повышение Д-димера до 1,69 мкг/мл (норма – до 0,5 мкг/мл).
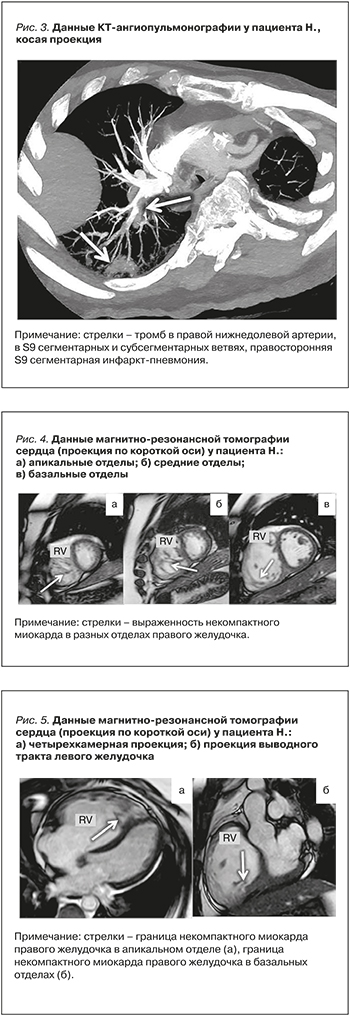 Ультразвуковое исследование (УЗИ) не выявило флотирующих тромбов или тромбоза глубоких вен нижних конечностей и малого таза. Диагностический поиск был продолжен с использованием мультиспиральной компьютерной томографии (МСКТ) органов грудной клетки с контрастированием. Наблюдались дефекты контрастирования в просвете правой междолевой и нижнедолевой артерий, в S9, 10 сегментарных и в S9 субсегментарных ветвях (рис. 2). Обнаружена окклюзия S9 субсегментарных ветвей с развитием инфаркт-пневмонии (рис. 3).
Ультразвуковое исследование (УЗИ) не выявило флотирующих тромбов или тромбоза глубоких вен нижних конечностей и малого таза. Диагностический поиск был продолжен с использованием мультиспиральной компьютерной томографии (МСКТ) органов грудной клетки с контрастированием. Наблюдались дефекты контрастирования в просвете правой междолевой и нижнедолевой артерий, в S9, 10 сегментарных и в S9 субсегментарных ветвях (рис. 2). Обнаружена окклюзия S9 субсегментарных ветвей с развитием инфаркт-пневмонии (рис. 3).
Магнитно-резонансная томография (МРТ) сердца выявила дилатацию предсердий и ПЖ (конечно-диастолический объем 200 мл), трикуспидальную регургитацию 3 ст., снижение глобальной сократительной способности ПЖ (фракция выброса ПЖ 35%; ударный объем ПЖ 40 мл). Отмечено утолщение миокарда в апикальном отделе и в латеральной стенке среднего отдела с четким разграничением на компактный и некомпактный слои (рис. 4а). В базальном отделе ПЖ наблюдалась граница распространения некомпактного слоя (рис. 4б). В диастолу толщина некомпактного слоя составила 36 мм, компактного слоя – 5 мм. Обнаружена некомпактность миокарда в апикальном отделе – 1:7,2 (рис. 5). На Т1-взвешенных изображениях в миокарде отсутствовали участки жировой инфильтрации. После контрастного усиления участков патологического сигнала в миокарде не наблюдалось.
ОБСУЖДЕНИЕ
Клинические особенности изолированной формы НМПЖ освещались в литературе мало. Сообщается прежде всего о тромбоэмболии легочной артерии (ТЭЛА) и внезапной смерти [10]. Описываются случаи бессимптомного течения, дисфункции ПЖ, аритмии и тахикардии [4, 7, 8]. Рекомендовано рассматривать ТЭЛА как ведущую причину летального исхода при НМПЖ [10]. Долгосрочных наблюдений пациентов с НМПЖ не проводилось [3].
Прижизненный диагноз некомпактного миокарда ставится преимущественно при ЭхоКГ и МРТ сердца. Указывается на высокую корреляцию результатов ЭхоКГ и МРТ при выявлении некомпактного миокарда [11]. Независимо от выбранной методики используются схожие диагностические критерии некомпактного миокарда ЛЖ [12].
При ЭхоКГ некомпактный миокард диагностируют на основании следующих признаков: наличие двухслойной структуры миокарда с истонченным компактным и утолщенным некомпактным слоем в соотношении ≥1:2,3; наличие многочисленных трабекул и крипт; снижение подвижности пораженных сегментов [1]. Предложена количественная оценка степени некомпактности миокарда: величина соотношения компактного и некомпактных слоев 0,33–0,26 расценивается как «мягкая» некомпактность, 0,25–0,2 – как умеренная, менее 0,2 – как тяжелая [13]. Степень некомпактности миокарда тесно коррелирует со скоростью развития сердечной недостаточности.
При ЭхоКГ возможны неоднозначные результаты вследствие их зависимости от акустического окна и неудовлетворительной визуализации верхушки ЛЖ и полости ПЖ [11]. В случаях, когда ультразвуковая картина сомнительна, предлагается проведение МРТ. К достоинствам МРТ относят точную оценку слоев миокарда, визуализацию полости ПЖ и верхушки ЛЖ [12].
При МРТ некомпактный миокард диагностируют на основе четырех показателей: соотношение некомпактного слоя к компактному ≥1:2,3 в конце диастолы или ≥1:2 в конце систолы; трабекулярная масса более 20%; количественная оценка трабекул апикального миокарда (фрактальная размерность) ≥1,392 [11].
В литературе отсутствуют данные о проведении исследований, посвященных изолированному НМПЖ и соответственно нет общепризнанных критериев его диагностики. Поэтому предлагается использовать критерии некомпактной кардиомиопатии, установленные для ЛЖ при оценке НМПЖ [5]. Нормой считается повышенная трабекулярность в апикальном отделе ЛЖ, патологией – наличие четырех или более трабекул апикально к папиллярным мышцам [3].
До настоящего времени не предложено конкретного критерия повышенной трабекулярности ПЖ; часто патологическую трабекулярность ошибочно принимают за индивидуальную норму [3]. О диагностике НМПЖ существуют противоречивые мнения. Одни исследователи отмечают, что известные диагностические критерии для оценки некомпактного слоя ПЖ не применимы, аргументируя это тем, что в норме могут встречаться массивные трабекулы [9]. Другие признают патологической повышенную трабекулярность латеральной стенки, достигающей межжелудочковой перегородки [3]. Для разрешения этих противоречий предлагается использовать косвенные признаки НМПЖ. В качестве таковых рекомендуется рассматривать дилатацию ПЖ (в тяжелых случаях с поражением трикуспидального клапана) [6], а также гистологический критерий: трабекулярность признается патологической при толщине некомпактного миокарда более 75% [2].
НМПЖ требует дифференциального диагноза с аритмогенной дисплазией правого желудочка (АДПЖ). В последнем случае наблюдаются Y-образные трабекулы, поэтому некомпактная и аритмогенная кардиомиопатии имеют визуальное сходство. Еще трудней определить их сосуществование [9]. АДПЖ характеризуется структурными изменениями и функциональными нарушениями ПЖ, приводящими к жизнеугрожающей желудочковой аритмии. Структурные изменения характеризуются жировой инфильтрацией и фиброзом миокарда ПЖ. Функциональные нарушения проявляются прогрессирующей дилатацией и дисфункцией ПЖ [14]. Для диагностики АДПЖ важны нарушения кинетики ПЖ и визуализация фиброзных изменений [14, 15].
Диагностика АДПЖ строится на больших и малых критериях, включающих 6 позиций [10]. К большим ЭКГ-критериям относят инвертированный Т-зубец и эпсилон-волны в правых грудных отведениях, желудочковую тахикардию с блокадой левой ножки пучка Гиса, частые (более 1000/сут) желудочковые экстрасистолы. Диагностические критерии АДГПЖ при ЭхоКГ и МРТ включают индекс конечно-диастолического объема >100–110 мл/м2, фракцию выброса ПЖ <40–45%, дилатацию выходного тракта ПЖ >32–36 мм, региональный акинез стенки либо дискинез при аневризматических изменениях. Более характерным признаком выступают поражение базальных отделов и задней стенки [14]. МРТ позволяет визуализировать жировые отложения и фиброзные изменения в миокарде, поэтому является более информативным методом диагностики при АДПЖ [15].
В представленном нами случае присутствовали клинические проявления НМПЖ – нарушения ритма и ТЭЛА. При этом были выявлены и другие признаки изолированного НМПЖ.
1. Трабекулы, проходящие от свободной стенки к межжелудочковой перегородке, и глубокие межтрабекулярные пространства, сообщающиеся с основной полостью ПЖ.
2. Компактный и некомпактный слои миокарда в апикальном отделе и в латеральной стенке ПЖ.
3. Соотношение компактного миокарда к толщине всей стенки 1:7,2, некомпактный слой – 88% толщины стенки.
4. Истончение компактной части стенки ПЖ менее 5 мм, наблюдавшееся в апикальных и частично в средних отделах, но не в базальных, как при аритмогенной дисплазии.
5. Дилатация и снижение фракции выброса ПЖ, что характерно как для некомпактной, так и аритмогенной кардиомиопатии.
6. Отсутствие интрамиокардиального отложения жира и постконтрастных фиброзных изменений, свойственных для АДПЖ.
7. Отсутствие признаков вовлечения стенки ЛЖ и сопутствующих сердечных аномалий.
8. Характерное для НМПЖ осложнение в виде ТЭЛА, легочная гипертензия (при ЭхоКГ), тромбоэмболия и инфаркт-пневмония (при МСКТ). При этом УЗИ не выявило тромбы в венах нижних конечностей как причину развития ТЭЛА.
Сочетание диагностических критериев некомпактной кардиомиопатии в нашем случае наблюдалось только в пораженном ПЖ, а отсутствие дифференциально-диагностических признаков АДПЖ позволило сделать заключение об изолированной форме НМПЖ. МРТ выявило изолированную форму НМПЖ в ситуации, когда наблюдалась сомнительная ультразвуковая картина: она позволила четко визуализировать все сегменты сердца, отграничить компактную и некомпактную части пораженного миокарда, оценить степень систолической дисфункции.



