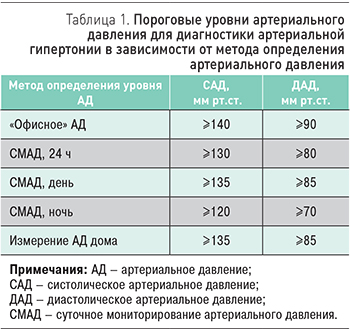
Артериальная гипертония (АГ) – состояние, при котором у беременных регистрируется систолическое артериальное давление (САД) ≥140 мм рт.ст. и/или диастолическое артериальное давление (ДАД) ≥90 мм рт.ст. При диагностике АГ необходимо подтвердить повышение уровня АД как минимум двумя измерениями с интервалом не менее 15 мин на той же руке. О наличии АГ при самостоятельном измерении АД беременной в домашних условиях или при проведении суточного мониторирования АД (СМАД) свидетельствует уровень АД ≥135/85 мм рт.ст.
РАСПРОСТРАНЕННОСТЬ
По данным The International Federation of Gynecology and Obstetrics (FIGO, 2016), АГ регистрируется у 5–10% беременных [1]. В Российской Федерации распространенность АГ у беременных составляет 7–30% [2]. По данным наблюдательного (обсервационного) исследования, проведенного в одном из перинатальных центров крупного города центральной части России (регистр беременных «БЕРЕГ»), гипертензивные нарушения регистрировались у 14% женщин [3].
На протяжении последнего десятилетия АГ и ассоциированные с ней осложнения занимают 4-е место в структуре причин материнской смертности с максимальным показателем у женщин в возрасте старше 35 лет. По данным Всемирной организации здравоохранения (ВОЗ), гипертензивные состояния при беременности в 2014 г. занимали 2-е место в структуре материнской смертности и были причиной не менее 76 тыс. случаев материнской и 500 тыс. случаев младенческой смертности ежегодно [2].
К наиболее значимым осложнениям беременности у пациенток с АГ относятся:
- плацентарная недостаточность;
- синдром задержки роста плода;
- антенатальная гибель плода;
- перинатальная смертность;
- преждевременная отслойка нормально расположенной плаценты;
- акушерские кровотечения;
- эклампсия;
- HELLP-синдром (гематома или разрыв печени);
- диссеминированное внутрисосудистое свертывание (ДВС-синдром);
- острое почечное повреждение;
- отек легких;
- нарушения мозгового кровообращения;
- кровоизлияние и отслойка сетчатки.
КЛАССИФИКАЦИЯ АРТЕРИАЛЬНОЙ ГИПЕРТОНИИ
Выделяют следующие клинические варианты АГ при беременности:
- АГ, имевшаяся до беременности, – хроническая АГ – гипертоническая болезнь (ГБ) или симптоматическая АГ;
- гестационная АГ;
- хроническая АГ, осложненная преэклампсией;
- преэклампсия/эклампсия.
Хроническая АГ (ХАГ) – повышение уровня АД ≥140/90 мм рт.ст., определяемое до наступления беременности или до 20 нед ее развития. АГ, диагностированная после 20 нед гестации и не исчезнувшая в течение 12 нед после родов, также классифицируется как существовавшая ранее АГ, но уже ретроспективно.
В группу ХАГ, помимо ГБ и симптоматической АГ, входят:
- гипертония «белого халата» – повышение АД при офисных измерениях ≥140/90 мм рт.ст. и АД <140/90 мм рт.ст. при самостоятельном (домашнем) измерении или при СМАД (среднесуточное АД <135/85 мм рт.ст.);
- маскированная АГ – АД <140/90 мм рт.ст. при офисном измерении и АД ≥140/90 мм рт.ст. при самостоятельном (домашнем) измерении или при СМАД (среднесуточное АД ≥135/85 мм рт.ст.).
Гестационная АГ (ГАГ) – состояние, индуцированное беременностью и проявляющееся уровнем АД ≥140/90 мм рт.ст. после 20 нед. В течение 12 нед после родов у пациенток с ГАГ АД возвращается к нормальному уровню. Если спустя 12 нед после родов АД сохраняется повышенным, то следует заподозрить ХАГ – ГБ или симптоматической АГ. ГАГ осложняет ≈6% беременностей.
ХАГ, осложненная преэклампсией, диагностируется в случае:
- появления у женщины с ХАГ протеинурии в количестве ≥0,3 г белка в суточной моче и/или
- заметного увеличения у женщины с ХАГ ранее имевшейся протеинурии и/или появления признаков полиорганной недостаточности.
Преэклампсия (ПЭ) – системный, специфичный для беременности синдром, вызывающий изменения в организме как матери, так и плода, развивающийся после 20-й недели беременности и характеризующийся повышением АД ≥140/90 мм рт.ст., протеинурией, а в ряде случаев и проявлениями полиорганной недостаточности. ПЭ рассматривают в настоящее время как острый эндотелиоз мелких артериальных сосудов, в результате которого изменяется баланс между тромбогенными и тромборезистентными свойствами сосудистой стенки в сторону увеличения тромбогенного потенциала, нарушаются реологические и коагуляционные свойства крови, что приводит к нарушениям микроциркуляции и микроангиопатиям [4].
Считают, что основными патогенетическими механизмами развития ПЭ служат нарушение инвазии трофобласта, дефекты гестационной перестройки спиральных артерий, кровоснабжающих плаценту, следствием чего становится ухудшение плацентарной перфузии и появление факторов широко распространенной эндотелиальной дисфункции с полиорганными системными проявлениями.
Эклампсия – приступ судорог или серия судорожных приступов на фоне преэклампсии при отсутствии других причин. В 30% случаев эклампсия развивается внезапно без предшествующей ПЭ.
ДИАГНОСТИКА АРТЕРИАЛЬНОЙ ГИПЕРТОНИИ
Основной метод диагностики АГ – измерение АД. Диагностировать АГ во время беременности следует на основании по крайней мере двух повышенных его значений с определенным интервалом.
Условия и правила измерения АД
- АД измеряют в состоянии покоя (через 10 мин после отдыха) 2 раза с интервалом в 1–2 мин. Если первые два значения существенно разнятся, измерения повторяют.
- Размер манжеты должен соответствовать размеру руки: при окружности плеча <33 см используется манжета стандартного размера (12/13 см), 33–41 см – манжета 15/33 см, >41 см – набедренная манжета 18/36 см. Несоблюдение этого требования может привести к искажениям результатов исследования на 30%.
- Плечо пациентки должно находиться на уровне IV–V межреберья. Нижний край манжеты должен быть на 2 см выше локтевого сгиба. Момент появления первых звуков соответствует I фазе тона Короткова и показывает САД; ДАД рекомендуют регистрировать в фазу V тона Короткова. У 15% беременных V фазу определить не удается, и в этих случаях уровень ДАД устанавливается по IV фазе, т.е. в момент значительного ослабления тонов.
- АД измеряют на обеих руках. Если оно разное, то ориентируются на более высокие его значения.
- У пациенток с сахарным диабетом (СД) АД необходимо измерять в положении сидя и лежа для исключения синдрома ортостатической гипотензии.
Известно, что среднесуточные значения АД имеют преимущества перед стандартными (офисными) показателями, так как более тесно коррелируют с поражением органов-мишеней и их динамикой на фоне лечения, позволяют предсказать появление протеинурии, риск преждевременных родов и в целом исходы беременности.
Показания к проведению СМАД у беременных:
- АГ;
- гипертония «белого халата»;
- маскированная АГ;
- заболевания почек (гломерулонефрит, хроническая болезнь почек);
- сахарный диабет 1 и 2 типа;
- тиреотоксикоз;
- тромбофилия, антифосфолипидный синдром (АФС);
- системная красная волчанка (СКВ);
- ожирение;
- преэклампсия.
СМАД проводят с помощью прибора для автоматической регистрации АД (приборы чаще осциллометрические) в течение 24 ч.
 При СМАД необходимо выполнять следующие условия:
При СМАД необходимо выполнять следующие условия:
- применять только приборы, валидированные с помощью стандартных протоколов;
- использовать манжеты адекватного размера и сравнивать начальные измерения с показаниями сфигмоманометра (разница не должна превышать пределов ±5 мм рт.ст.);
- регистрировать АД не реже чем каждые 30 мин, чтобы зафиксировать адекватное число значений и обеспечить репрезентативность, если какие-либо значения придется исключить из-за артефактов;
- скорость автоматического снижения давления в манжете должна быть <2 мм рт.ст.;
- пациентка должна вести нормальный образ жизни, при этом ей необходимо избегать чрезмерной нагрузки;
- во время измерения АД рука должна быть вытянута и находиться в спокойном положении;
- параллельно пациентка должна вести дневник, фиксируя в нем свою активность, продолжительность и качество сна;
- если из-за артефактов исключается >30% измеренных значений АД, то следует провести повторное СМАД. Процент адекватных показателей должен быть сопоставим в течение дня и ночи;
- необходимо помнить, что результаты амбулаторного мониторирования АД на несколько мм рт.ст. ниже офисных значений (табл. 1).
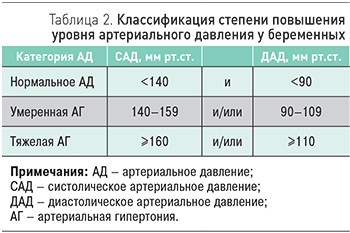 Классификация уровня АД по степени повышения у беременных, рекомендованная в настоящее время во многих странах мира, отличается от градаций уровня АД для женщин вне периода беременности (табл. 2). Данная классификация может использоваться для характеристики степени повышения уровня АД при любой форме АГ в период беременности – ХАГ, ГАГ, преэклампсии.
Классификация уровня АД по степени повышения у беременных, рекомендованная в настоящее время во многих странах мира, отличается от градаций уровня АД для женщин вне периода беременности (табл. 2). Данная классификация может использоваться для характеристики степени повышения уровня АД при любой форме АГ в период беременности – ХАГ, ГАГ, преэклампсии.
Выделение двух степеней АГ при беременности – умеренной и тяжелой – имеет принципиальное значение для оценки прогноза, тактики лечения и выбора метода родовспоможения.
У пациенток с ХАГ важную роль играет оценка общего сердечно-сосудистого риска, степень которого зависит не только от степени повышения уровня АД, но и от наличия сопутствующих факторов риска, поражения органов-мишеней и ассоциированных клинических состояний (табл. 3).

Наличие поражения органов-мишеней (ПОМ) и ассоциированных клинических состояний (АКС) определяют стадию ГБ:
- I стадия – отсутствие ПОМ;
- II стадия – поражение одного или нескольких органов-мишеней: сердца, сосудов, почек;
- III стадия – наличие АКС.
Как уже отмечалось, такой клинический вариант АГ при беременности, как ПЭ, может протекать с проявлениями полиорганной недостаточности/органной дисфункции у матери. К таким проявлениям относятся:
- со стороны ЦНС – сильная головная боль, гиперрефлексия, парестезии, фотопсии, слепота, изменение психического статуса, инсульт, эклампсия;
- со стороны ЖКТ – боль в правом подреберье или в эпигастрии, боль в животе, изжога, тошнота, рвота, повышенный уровень аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), лактатдегидрогеназы, билирубина;
- со стороны мочевыделительной системы – олигурия, анурия, креатинин >90 мкмоль/л;
- со стороны сердечно-сосудистой системы – снижение сатурации кислорода и клинические признаки гипоксии, отек легких, ишемия или инфаркт миокарда;
- со стороны гемостаза и кроветворной системы – повышение активированного частичного тромбопластинового времени (АЧТВ), международного нормализованного отношения (МНО), ДВС-синдром, снижение количества тромбоцитов <100×109/л, гемолиз;
- со стороны плода – маловодие, нарушение маточно-плацентарного кровотока 2–3 степени, синдром задержки роста плода, антенатальная гибель плода.
Наличие отеков НЕ является диагностическим критерием ПЭ. При физиологически протекающей беременности частота отеков достигает 50–80%. Вместе с тем при резком нарастании генерализованных отеков следует проявлять настороженность в отношении развития ПЭ, так как это может быть доклиническим или манифестным проявлением тяжелой ПЭ [5].
Выделяют 2 клинические формы ПЭ – умеренную и тяжелую, основные критерии которых представлены в табл. 4 [6].
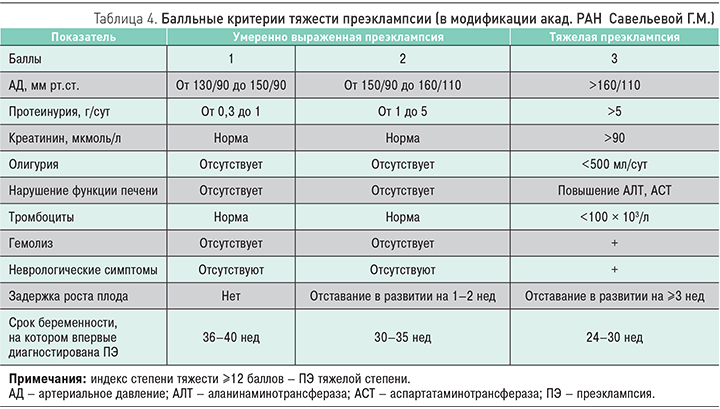
Использование балльной системы оценки степени тяжести ПЭ способствует правильной оценке вклада каждого фактора в диагноз и определяет тактику ведения пациентки.
«Золотым» стандартом для диагностики протеинурии является количественное определение белка в суточной порции мочи (С). Клинически значимой протеинурией во время беременности считают наличие белка ≥0,3 г/л в суточной пробе (24 ч) либо в двух пробах, взятых с интервалом в 6 ч (уровень доказательности B, класс рекомендаций 2b); при использовании тест-полоски (белок в моче) – показатель «1+» (В–2a) [7]. Критерием тяжелой ПЭ служит протеинурия 5,0 г/л в суточной пробе мочи или >3 г/л в двух порциях мочи, взятых с интервалом в 6 ч, или значение «3+» по тест-полоске [8].
При наличии симптомов критического состояния (тяжелая АГ, тромбоцитопения, церебральная, почечная, печеночная дисфункция, отек легких) наличие протеинурии необязательно для постановки диагноза «ПЭ тяжелой степени» [9].
ТАКТИКА ВЕДЕНИЯ БЕРЕМЕННЫХ С ПРЕЭКЛАМПСИЕЙ
Этапность оказания медицинской помощи при тяжелой ПЭ/эклампсии определяется Клиническими рекомендациями (протоколом лечения), утвержденными Минздравом России [10]. В соответствии с ними ПЭ/эклампсия является показанием для госпитализации в стационар 3 уровня.
Беременные с ПЭ умеренной степени должны наблюдаться в условиях отделения патологии беременности в учреждениях 2–3-го уровня совместно акушером-гинекологом и терапевтом (кардиологом), при этом возможно пролонгирование беременности. Досрочное родоразрешение показано при ухудшении состояния матери и/или плода.
Беременные с ПЭ тяжелой степени должны наблюдаться в условиях отделения интенсивной терапии в учреждениях 3-го уровня совместно акушером-гинекологом, анестезиологом-реаниматологом и терапевтом (кардиологом), а при необходимости еще и неврологом.
При ПЭ тяжелой степени решение вопроса о досрочном родоразрешении проводится при стабилизации состояния матери, после проведения профилактики респираторного дистресс-синдрома плода при сроке беременности менее 34 нед.
При стабилизации состояния беременной, эффективном ответе на антигипертензивную терапию и отсутствии признаков нарушения жизнедеятельности плода при сроке гестации менее 28 нед производится перерасчет критериев ПЭ. При оценке состояния беременной, данных лабораторного и инструментального обследований, подсчете баллов, соответствующих ПЭ умеренной степени, возможно пролонгирование беременности в интересах плода в условиях отделения патологии беременности при ежедневном лабораторном и инструментальном мониторировании соответствующих параметров.
Показания к экстренному (минуты) родоразрешению:
- кровотечение из родовых путей, подозрение на отслойку плаценты;
- острая гипоксия плода на сроке беременности более 22 нед.
Показания к срочному (часы) родоразрешению:
- постоянная головная боль и зрительные проявления;
- постоянная эпигастральная боль, тошнота или рвота;
- прогрессирующее ухудшение функции печени и/или почек;
- эклампсия;
- АГ, не поддающаяся медикаментозной коррекции;
- количество тромбоцитов <100 × 109/л и прогрессирующее его снижение.
Медикаментозная терапия ПЭ
- Профилактика и лечение судорог. На догоспитальном этапе необходимо оценить тяжесть ПЭ, обеспечить венозный доступ (катетеризация периферической вены), начать введение 25%-ного магния сульфата в количестве 16 мл внутривенно медленно в течение 10–15 мин, затем 100 мл через шприцевой насос со скоростью 4 мл/ч (1 г/ч в пересчете на сухое вещество), с продолжением введения препарата в условиях отделения интенсивной терапии.
- Антигипертензивна терапия. Проводится препаратами, рекомендованными к применению у беременных (см. ниже).
Профилактика ПЭ у беременных высокого и умеренного риска
К группе высокого риска развития ПЭ относятся пациентки, имеющие экстрагенитальные заболевания: ХАГ и другие гипертензивные нарушения во время предыдущей беременности, хронические заболевания почек, аутоиммунные заболевания – СКВ или АФС, СД 1 или 2 типа.
К факторам умеренного риска развития ПЭ относятся первая беременность, возраст 40 лет или старше, интервал между родами более 10 лет, индекс массы тела (ИМТ) ≥35 кг/м2 до настоящей беременности, семейный анамнез ПЭ, многоплодная беременность.
У беременных с высоким риском развития ПЭ возможен прием ацетилсалициловой кислоты (аспирина) в дозе 75–162 мг/сут с 12-й недели беременности: он признан безопасным для матери и плода (не вызывает тератогенный эффект, не увеличивает частоту самопроизвольных абортов). Не было получено доказательств увеличения клинически значимых кровотечений у матери при применении аспирина [11–13]. Вместе с тем при назначении этого лекарственного средства необходимо письменное информированное согласие женщины, так как в РФ в соответствии с инструкциями к препаратам, содержащим ацетилсалициловую кислоту, их прием противопоказан в I и III триместрах беременности.
Беременным с низким содержанием кальция в диете (<600 мг/сут) может быть рекомендован дополнительный прием этого макроэлемента в количестве >1,0 г/сут; это не только вдвое уменьшает риск развития ПЭ, но и снижает материнскую заболеваемость и смертность в группах высокого риска [14, 15]. Следует принять во внимание, что среднее потребление кальция в России составляет 500–750 мг/сут. Согласно современным нормам, физиологическая потребность беременных в нем составляет от 1000 мг/сут, а в возрасте моложе 19 лет – 1300 мг/сут [16].
ПЛАНИРОВАНИЕ БЕРЕМЕННОСТИ ПАЦИЕНТКАМИ С ХРОНИЧЕСКОЙ АРТЕРИАЛЬНОЙ ГИПЕРТОНИЕЙ
Женщины с ХАГ при планировании беременности должны пройти комплексное клинико-лабораторное обследование, которое подчинено следующим целям:
- оценке функционального состояния органов-мишеней – электрокардиография (ЭКГ), эхокардиография (ЭхоКГ), СМАД, исследование сосудов глазного дна, ультразвуковое исследование (УЗИ) почек, при необходимости мониторирование ЭКГ по Холтеру, нагрузочные тесты, анализы крови и мочи, биохимическое исследование крови с определением глюкозы, липидограммы, электролитов, общего белка, АСТ, АЛТ, щелочной фосфатазы, мочевины, мочевой кислоты, креатинина;
- определению степени АГ и стадии ГБ;
- коррекции антигипертензивной терапии в случае ее применения;
- оценке прогноза для матери и плода.
На прегравидарном этапе рекомендовано выделять категорию пациенток с «высоким нормальным» АД – САД 130–139 мм рт.ст. и/или ДАД 85–89 мм рт.ст., что служит показанием для консультации кардиолога.
Пациенткам с АГ необходимо отменить препараты, противопоказанные при беременности, такие как атенолол, ингибиторы АПФ, антагонисты рецепторов ангиотензина II, антагонисты альдостерона (спиронолактон), антагонисты рецепторов к минералокортикоидам (эплеренон), резерпин, недигидропиридиновые антагонисты кальция. Если женщина принимала статины или аспирин, то на этапе прегравидной подготовки или сразу же при наступлении беременности эти препараты также необходимо отменить.
ЛЕЧЕНИЕ АРТЕРИАЛЬНОЙ ГИПЕРТОНИИ У БЕРЕМЕННЫХ
Целью лечения АГ у беременных является предупреждение осложнений, связанных с повышением АД, сохранение беременности, нормальное развитие плода и своевременное родоразрешение.
Немедикаментозные методы
Меры по немедикаментозному снижению АД следует рекомендовать всем пациенткам независимо от тяжести АГ и лекарственной терапии. К этим мерам относятся:
- прекращение курения;
- нормальная сбалансированная диета без ограничения потребления поваренной соли и жидкости;
- умеренная аэробная физическая нагрузка, достаточный 8–10-часовой ночной сон, желательно 1–2-часовой дневной сон.
Снижение массы тела в период беременности не рекомендуется в связи с риском рождения детей с низким весом и последующим замедлением их роста.
Критерии допустимой физиологической прибавки в весе у женщины за период гестации в зависимости от ИМТ до беременности отражены в табл. 5 [17].
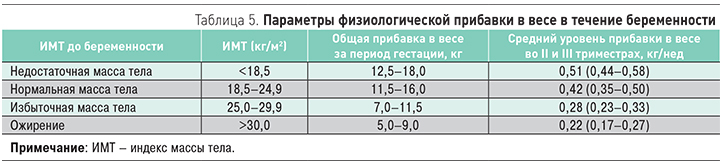
Следует подчеркнуть, что ожирение у матери может быть причиной неблагоприятных исходов как для нее самой, так и для плода.
Лекарственная терапия
Общими принципами медикаментозного лечения АГ являются:
- максимальная эффективность для матери и безопасность для плода;
- начало лечения с минимальных доз одного препарата;
- переход к препаратам другого класса при недостаточном эффекте (после увеличения дозы первого препарата) или плохой его переносимости;
- назначение комбинированной терапии препаратами из разных классов при недостаточном эффекте;
- использование препаратов длительного действия для достижения 24-часового эффекта при однократном/двукратном приеме. Применение таких препаратов обеспечивает более мягкое и длительное антигипертензивное действие, более интенсивную защиту органов-мишеней, а также повышает приверженность пациенток лечению.
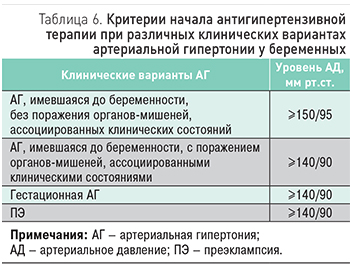 При умеренной АГ (140–159/90–109 мм рт.ст.) в клинических испытаниях не была доказана польза проводимой антигипертензивной терапии (АГТ): не выявлено снижения риска развития ПЭ, перинатальной смертности, преждевременных родов, рождения маловесных детей. Вместе с тем лечение умеренной АГ предупреждает развитие тяжелой АГ. Критерии начала АГТ при различных вариантах течения АГ у беременных представлены в табл. 6.
При умеренной АГ (140–159/90–109 мм рт.ст.) в клинических испытаниях не была доказана польза проводимой антигипертензивной терапии (АГТ): не выявлено снижения риска развития ПЭ, перинатальной смертности, преждевременных родов, рождения маловесных детей. Вместе с тем лечение умеренной АГ предупреждает развитие тяжелой АГ. Критерии начала АГТ при различных вариантах течения АГ у беременных представлены в табл. 6.
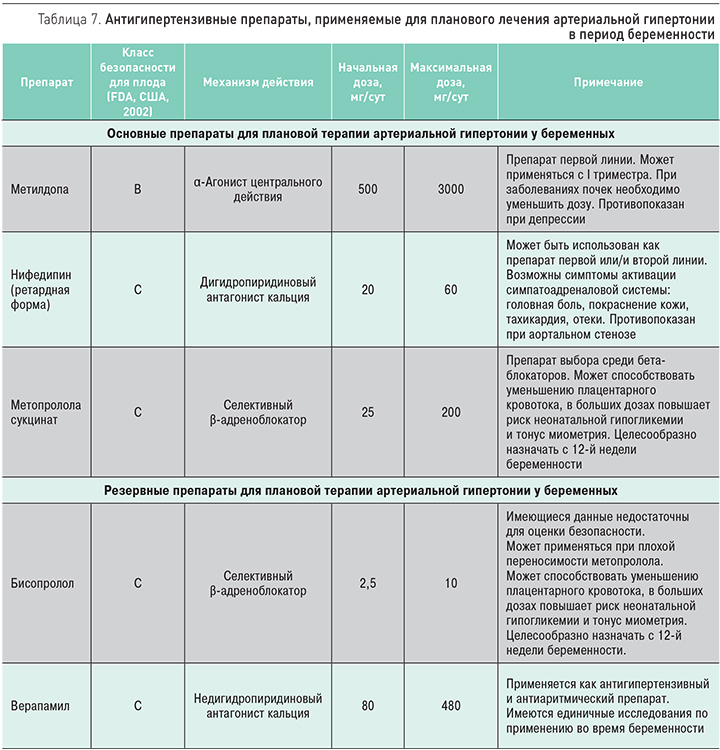
Для медикаментозного лечения АГ при беременности применяют небольшой спектр лекарственных средств, отвечающих критериям безопасности для плода (табл. 7).
Комбинированная терапия проводится в случае неэффективности монотерапии в максимальной дозе. Рациональной комбинацией является нифедипин длительного действия + β-адреноблокатор (β-АБ).
Лечение ГАГ (после 20 нед гестации) проводится в акушерском стационаре 2–3 уровня. При получении хорошего эффекта от лечения (нормализация АД, отсутствие протеинурии, удовлетворительное состояние матери и плода) оно может быть продолжено амбулаторно, при недостаточном эффекте терапии беременная должна находиться в стационаре до родоразрешения.
Родоразрешение
АГ сама по себе не служит показанием к абдоминальному родоразрешению, при удовлетворительном состоянии матери и плода и отсутствии акушерских показаний к кесареву сечению целесообразно родоразрешение через естественные родовые пути. При ведении родов у этого контингента женщин в день родоразрешения следует продолжать плановую антигипертензивную терапию. Во время родов возможно применение как β-АБ, так и антагонистов кальция, а также препаратов центрального действия.
С целью обезболивания следует использовать эпидуральную анестезию, которая обеспечивает не только эффективное обезболивание родов, но и дополнительный гипотензивный эффект. При недостаточной эффективности лечения в периоде изгнания плода рекомендуется исключение потуг.
Лечение АГ в послеродовом периоде
В послеродовом периоде даже у нормотензивных женщин наблюдается тенденция к повышению АД, которое достигает максимальных величин на 5-й день после родов, что является следствием физиологического увеличения объема жидкости и мобилизации ее в сосудистое русло. У пациенток с АГ сохраняется такая же тенденция. Выбор лекарственного средства в послеродовом периоде во многом определяется кормлением грудью, но в целом рекомендованы те же лекарственные средства, которые женщина получала во время беременности и после родов. Следует, однако, подчеркнуть, что диуретики (фуросемид, гидрохлоротиазид, спиронолактон) могут уменьшать продукцию молока.
Тактика лечения АГ после родов
- При АГ без ПОМ, АКС и уровне АД <150/95 мм рт.ст. после родов оправдан отказ от медикаментозной терапии. Лактация при этом возможна.
- При АГ без ПОМ, АКС и уровне АД 150/95–179/109 мм рт.ст. рекомендована низкодозированная фармакотерапия, что позволяет продолжить кормление грудью. В этой ситуации целевых значений АД, вероятно, достичь не удастся, однако общий сердечно-сосудистый риск будет снижен.
- У пациенток из группы высокого риска (АГ с ПОМ и/или АКС при уровне АД ≥180/110 мм рт.ст., СД, метаболическом синдроме) целесообразна антигипертензивная терапия, в том числе комбинированная, с достижением целевого уровня АД. В этой ситуации необходим отказ от кормления грудью.
Тактика лечения АГ в период лактации
Рекомендации по ведению пациенток с АГ в течение 12 нед после родов включают следующие положения:
- АД должно быть измерено сразу после родов и контролироваться в течение 3–6 дней после родов.
- У женщин с послеродовой АГ должна быть исключена ПЭ.
- Антигипертензивная терапия в послеродовом периоде должна быть продолжена, особенно у женщин с ПЭ и при рождении недоношенных детей.
- В качестве антигипертензивных препаратов целесообразно использовать нифедипин длительного действия, метилдопу, метопролол, бисопролол.
По прошествии 12 нед после родов пациенткам с АГ рекомендовано:
- При ГБ или стойкой послеродовой АГ пройти следующее обследование (если не сделано ранее): общий анализ крови и мочи, биохимическое исследование крови с определением натрия, калия, креатинина, глюкозы, холестерина, триглицеридов и липидного профиля, ЭКГ.
- При тяжелой ПЭ (особенно до 34 нед) необходимо обследование с целью исключения ГБ или симптоматической АГ.
- При перенесенной ПЭ, трудно контролируемой послеродовой АГ, сохранении протеинурии в течение 3–6 мес после родов, снижении СКФ <60 мл/ мин или других признаках заболевания почек (мочевой осадок) консультация терапевта или нефролога.
- При избыточном весе или ожирении снижение массы тела для уменьшения риска развития осложнений при следующих беременностях и для первичной профилактики сердечно-сосудистых заболеваний (ССЗ).
Отдаленный риск развития ССЗ у женщин, имевших АГ во время беременности
Все больше данных свидетельствует о том, что гипертензивные нарушения во время беременности выступают фактором риска развития ССЗ в будущем. Пациентки с ПЭ имеют 3–4-кратный риск развития АГ в будущем, 2-кратный риск развития ИБС и повышенный риск инсульта по сравнению с женщинами без ПЭ в анамнезе; самый высокий риск отмечался у женщин с ранней ПЭ (роды до 32 нед), мертворождением или внутриутробной задержкой роста плода [18]. Встречаются немногочисленные исследования, посвященные изучению влияния АГ у беременных на отдаленный прогноз для ребенка. Установлено, что весо-ростовые показатели новорожденного и степень раннего постнатального роста ребенка могут дать представление о будущих антропометрических параметрах взрослого и предсказать вероятность развития ожирения, СД 2 типа и ССЗ в последующем [19, 20]. Известно, что у женщин с АГ в периоде беременности чаще рождаются дети с низким весом. Данные когортного исследования, проведенного в Великобритании, показали отрицательную корреляцию между весом при рождении и значениями САД у наблюдаемых пациентов в возрасте 36–53 лет [21].
Результаты еще одного исследования, опубликованные в 2003 г., свидетельствуют о том, что 12-летние дети, родившиеся от матерей с ПЭ, имеют достоверное повышение уровня АД и концентрации эпинефрина в крови [22]. Результаты большого регистра в Норвегии, включавшего более 400 тыс. пациентов, выявили ассоциацию ПЭ с развитием бронхиальной астмы у ребенка [23].
Соответственно женщины с различными клиническими вариантами АГ при беременности в послеродовом периоде и в последующие годы должны регулярно контролировать АД и метаболические факторы риска: им рекомендуется модификация образа жизни для профилактики осложнений при последующих беременностях и снижения риска сердечно-сосудистых исходов в будущем.
Тактика ведения пациенток с гипертоническим кризом
Течение АГ может осложниться гипертоническим кризом (ГК) – быстрым, дополнительным, значительным подъемом АД, который может быть спровоцирован физической и психической нагрузкой, приемом большого количества соли, жидкости, отменой медикаментозного лечения. Повышение АД до ≥170/110 мм рт.ст. требует неотложных госпитализации (желательно в отделение интенсивной терапии с целью постоянного мониторинга АД и парентерального введения препаратов для быстрого снижения АД) и медикаментозной терапии (табл. 8).
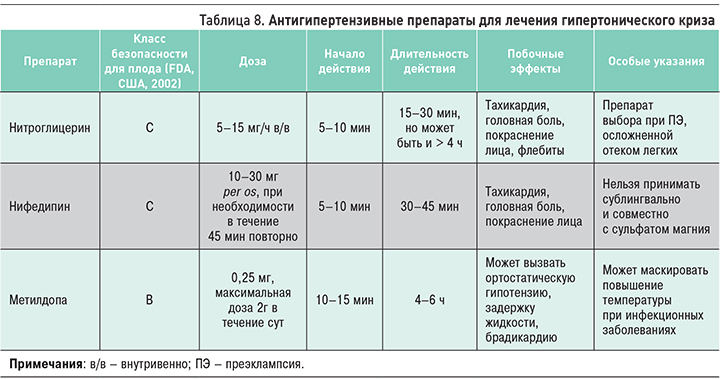
При лечении ГК внутривенное введение препаратов безопаснее и предпочтительнее, чем пероральный или внутримышечный способы применения, так как позволяет предупредить развитие тяжелой гипотензии прекращением инфузии.
АД необходимо снижать на 25% от исходного уровня в течение первых двух часов и до нормализации его уровня в последующие 2–6 ч.



