ВВЕДЕНИЕ
Антикоагулянтная терапия – важнейшая составляющая в профилактике тромботических и тромбоэмболических осложнений у пациентов, перенесших ортопедические хирургические вмешательства [1]. За счет разработки и внедрения в клиническую практику прямых ингибиторов факторов свертывания крови для перорального приема удалось значимо снизить риск венозных тромбоэмболических осложнений (ВТЭО). Эти препараты не требуют рутинного контроля свертывания крови [2–4]. Вместе с тем у пациентов со скрытыми нарушениями в системе гемостаза применение ривароксабана и апиксабана может сопровождаться повышенным риском развития интраоперационного и послеоперационного кровотечения. Особенно актуальна данная проблема у больных травматолого-ортопедического профиля, так как объемные ортопедические вмешательства могут сопровождаться значительной кровопотерей [5]. Это обстоятельство обусловливает необходимость оценки вероятности возникновения кровотечения у пациентов, получающих прямые оральные антикоагулянты, не требующие регулярного мониторинга коагуляции [6].
В настоящее время универсального теста для оценки антикоагулянтной активности прямых ингибиторов факторов свертывания, кроме определения концентрации ривароксабана и апиксабана в крови, нет, причем последнее исследование доступно лишь единичным лабораториям [5]. В повседневной практике следует учитывать совокупность клинических признаков и результатов коагулологических, биохимических и гематологических анализов [7].
Цель предлагаемого исследования – сравнить коагулологические, биохимические и гематологические лабораторные показатели при приеме ривароксабана и апиксабана у больных с остеоартритом после эндопротезирования тазобедренного сустава.
МАТЕРИАЛ И МЕТОДЫ
Дизайн работы: проспективное динамическое сравнительное исследование.
В исследование были включены 38 пациентов, находившихся в клинике травматологии и ортопедии ФГБОУ ВО «Северо-Западный государственный университет им. И.И. Мечникова» Минздрава России c диагнозом «остеоартрит тазобедренного сустава» для выполнения планового эндопротезирования тазобедренного сустава (ЭТБС). Критериями исключения служили острые воспалительные и инфекционные заболевания, включая COVID-19, сердечно-сосудистые заболевания в стадии субкомпенсации, болезни почек (клиренс креатинина менее 50 мл/мин), дыхательная недостаточность, онкологические заболевания.
Средний возраст пациентов составил 58±15 (33; 85) лет. В зависимости от проводимой терапии, пациенты были разделены на 2 группы:
- первая группа – 25 пациентов (12 женщин и 13 мужчин), получавших ривароксабан (10 мг 1 раз/сут) в течение 7 дней;
- вторая группа – 13 пациентов (6 женщин и 7 мужчин), получавших апиксабан (2,5 мг 2 раза/ сут) в течение того же времени.
Исследование было одобрено этическим комитетом ФГБОУ ВО «Северо-Западный государственный университет им. И.И. Мечникова» Минздрава России и проводилось в соответствии с этическими стандартами, изложенными в Хельсинкской декларации. Все обследованные лица дали добровольное информированное согласие на участие в исследовании.
Всем больным были выполнены лабораторные исследования до операции (исходно), после операции (на фоне приема антикоагулянта) и на 7-е сутки после проведения ЭТБС. Лабораторное исследование включало определение показателей гемостаза (международное нормализированное отношение, активированное частичное тромбопластиновое время, фибриноген, D-димер) на анализаторе STA Compact (Stago, Франция), биохимических показателей (кальций общий, кальций ионизированный, сывороточное железо, С-реактивный белок) на анализаторе COBAS Integra 400plus и гематологических параметров на анализаторе LH-500 (Beckman Coulter, США).
Концентрацию ривароксабана и апиксабана определяли в плазме крови на анализаторе ACL TOP 500CTS (Werfen, США) в первые сутки после операции и на 7-е сутки после ЭТБС. Все методики проводились по соответствующим инструкциям к наборам и анализаторам. Характеристика фармакокинетических и фармакодинамических свойств ривароксабана и апиксабана, а также особенности применения препаратов представлены в таблице 1.
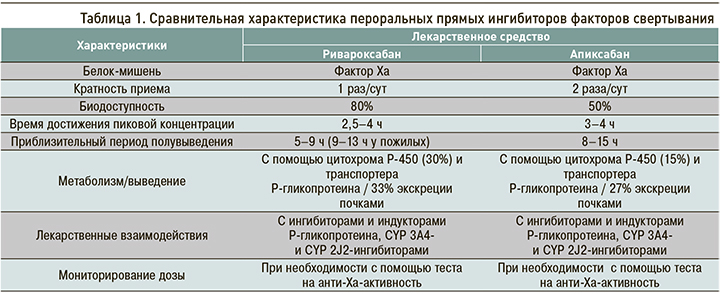
К преимуществам ривароксабана можно отнести его однократное применение, что способствует не только приверженности пациентов к лечению, но и профилактике кровотечений [8].
Статистическая обработка данных в рамках исследования осуществлялась с помощью статистической программы Jamovi. Числовые значения представлены в виде медианы Мe, 25-го и 75-го перцентилей. Для сравнения связанных количественных показателей использовался критерий Фридмана. Корреляции между показателями определяли по Спирмену. Различия считались статистически значимыми при р <0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При поступлении у всех пациентов лабораторные показатели гемостаза, гематологические и биохимические маркеры находились в пределах референтных значений, кроме фибриногена, концентрация которого во 2-й группе была выше 4,53 (3,05; 4,93) г/л.
Оценка остаточного антикоагулянтного эффекта прямых ингибиторов фактора Ха (ривароксабана и апиксабана) выполнялась путем определения концентрации препарата в плазме крови. Определялась эффективность действия по максимальной концентрации (Сmax) лекарственного средства в плазме (взятие крови осуществлялось в момент достижения предполагаемой максимальной концентрации). У пациентов, получавших ривароксабан, в первый день после ЭТБС в плазме крови средняя Сmax препарата составила 122,4 нг/ мл (94; 178) и при выписке – 186,47 (152,8; 239) нг/мл, что соответствовало терапевтическим интервалам. Для апиксабана аналогичные показатели равнялись 60,3 (14; 95,2) и 79,85 (14; 196,4) нг/мл, что также соответствовало терапевтическим интервалам.
После операции при анализе показателей системы гемостаза у пациентов (табл. 2), получавших ривароксабан и апиксабан, было выявлено достоверное повышение концентрации фибриногена и D-димера по сравнению с исходными данными, что было обусловлено хирургическим вмешательством. У пациентов на фоне приема ривароксабана наблюдалось статистически значимое повышение международного нормализированного отношения (МНО, р <0,05) в отличие от группы пациентов, получавших апиксабан. Однако, по данным различных авторов, не существует унифицированного коагулологического теста, который указывал бы на эффективность антикоагулянтной активности ривароксабана или апиксабана [9, 10].
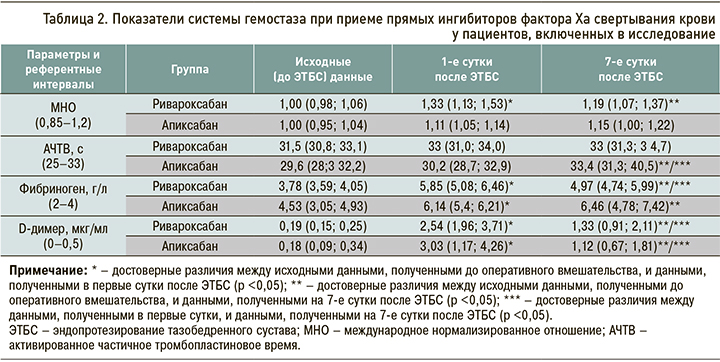
На 7-е сутки после хирургического вмешательства содержание D-димера достоверно снизилось как в группе ривароксабана, так и апиксабана, но не достигло референтных интервалов, тогда как показатели фибриногена и активированного частичного тромбопластинового времени (АЧТВ) у пациентов, получавших апиксабан, оставались высокими. Повышение фибриногена как белка острой фазы может быть обусловлено имевшим место воспалительным процессом. Таким образом, у пациентов, принимавших апиксабан, в процессе терапии воспалительная реакция не уменьшилась.
При сравнении уровней С-реактивного белка (СРБ), полученных исходно и в первые сутки после оперативного вмешательства, наблюдалось статистически значимое его повышение в обеих группах. На 7-е сутки после ЭТБС концентрация СРБ у пациентов, получавших апиксабан, оставалась высокой, тогда как в группе ривароксабана она была достоверно ниже в сравнении с концентрацией сразу после операции (табл. 3). Таким образом, в группе пациентов, принимавших апиксабан, СРБ, служащий маркером воспаления, был выше, чем в группе ривароксабана.
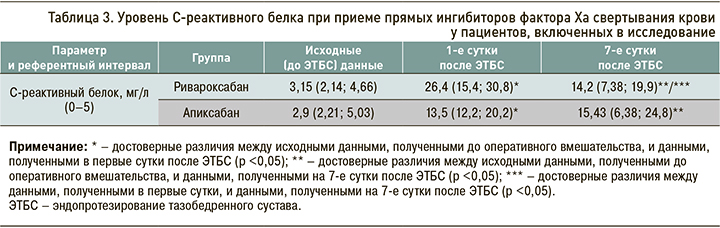
Таким образом, новые пероральные антикоагулянты ривароксабан и апиксабан обеспечивали благоприятное соотношение риска и пользы при приеме у пациентов после ЭТБС, что подтверждается литературными данными об использования этих лекарственных средств у пациентов, перенесших ортопедические оперативные вмешательства [11]. Оба препарата показали высокую эффективность и безопасность в отношении развития кровотечений [12]. В то же время, по результатам нашего исследования, у пациентов, получавших апиксабан, показатели воспаления были выше, чем в группе пациентов, применявших ривароксабан.
Опираясь на результаты исследований, посвященных новым оральным антикоагулянтам [13–16], а также данные, полученные в ходе нашей работы, можно сделать вывод, что для пациентов, перенесших ЭТБС, предпочтителен прием ривароксабана в сравнении с апиксабаном.
ЗАКЛЮЧЕНИЕ
При применении ривароксабана и апиксабана у больных после ЭТБС не наблюдалось геморрагических осложнений. Оценка концентрации этих препаратов в плазме крови показала эффективность их антикоагулянтного действия и подтвердила необходимость их приема для профилактики тромботических осложнений при высоком риске таких осложнений у пациентов после тотальной артропластики тазобедренного сустава. Учитывая полученные в этой работе данные при сопоставлении показателей гемостаза и СРБ в группах пациентов, получавших указанные прямые ингибиторы фактора Ха свертывания крови, с целью снижения воспалительной реакции можно считать предпочтительным использование ривароксабана.



