Бронхиальная астма (БА) – одно из самых часто встречающихся хронических заболеваний человека. Низкие официальные показатели заболеваемости БА в России, составляющие, по данным статистики, 1–2 % населения страны, не отражают истинную картину ее распространенности. Проведенные эпидемиологические исследования свидетельствуют о значительно более высоком уровне заболеваемости, согласно которым БА в России страдает около 7% взрослого населения [1, 2].
Одной из причин гиподиагностики БА служит ошибочная трактовка клинических проявлений заболевания, когда диагноз устанавливается только при обязательном наличии приступов экспираторного удушья, в то время как другие респираторные симптомы – эпизоды дыхательного дискомфорта, затрудненного дыхания на выдохе, приступообразный кашель, сухие свистящие хрипы – рассматриваются в качестве проявлений хронического обструктивного бронхита (хронического бронхита с обструктивным компонентом, астматического бронхита, предастмы). Кроме того, у взрослых пациентов в период стойкой ремиссии заболевания часто не учитывается диагноз БА, установленный в детском возрасте и расцениваемый как излеченный. В силу вариабельности течения БА вне обострения заболевания возможно полное отсутствие симптомов.
Цель этой статьи – представить методические рекомендации для терапевтов и врачей общей практики по диагностике БА у взрослых пациентов.
ПАТОГЕНЕЗ, КЛИНИКА, АНАМНЕЗ ПРИ БРОНХИАЛЬНОЙ АСТМЕ
БА – гетерогенное заболевание, характеризующееся хроническим воспалением дыхательных путей и проявляющееся варьирующими во времени и по интенсивности респираторными симп-томами, такими как свистящие хрипы, одышка, заложенность в груди, кашель, и вариабельной обструкцией дыхательных путей [3, 4].
Согласно современной концепции, в основе патогенеза БА, вне зависимости от степени тяжести заболевания, лежит хронический воспалительный процесс (преимущественно эозинофильное воспаление) в стенке бронхов, приводящий к спазму, отеку слизистой, гиперсекреции слизи и бронхиальной обструкции в ответ на воздействие различных триггерных факторов, к которым относятся специфические аллергены клещей домашней пыли, животных, таракана, плесневых грибов, пыльцы растений и профессиональных сенсибилизаторов и большая группа неспецифических факторов, таких как аэрополлютанты (озон, диоксид серы и азота, продукты сгорания дизельного топлива), респираторные инфекции, физическая нагрузка, гипервентиляция, вдыхание холодного воздуха, курение (активное и пассивное), ирританты (бытовые аэрозоли, резкие запахи). Длительное неконтролируемое воспаление при БА приводит к ремоделированию бронхов и, как следствие, к необратимой обструкции [3–5].
Диагноз БА является сугубо клиническим и основывается на жалобах пациента, детальном анамнезе и результатах обследований, прежде всего подтверждающих факт обратимой обструкции бронхов. Также проводится дифференциальная диагностика, которая исключает наличие иного заболевания дыхательных путей, схожего по симп-томатике с БА.
Важнейшим звеном диагностики БА выступает тщательный сбор анамнеза: выяснение причин возникновения, длительности, вариабельности симптомов, наличие аллергических реакций у пациента и его кровных родственников, причинно-следственные особенности появления симптомов болезни и ее обострений [3].
При сборе анамнезе необходимо уточнить наличие следующих симптомов:
- эпизоды хрипов или свистов в грудной клетке, чувства затруднения дыхания, сухого приступообразного кашля;
- усиление симптомов преимущественно ночью и рано утром;
- усиление симптомов при физической нагрузке;
- появление симптомов при контакте с аллергенами (пыль, животные, пыльца растений, плесневые грибы);
- появление симптомов при вдыхании холодного воздуха, резких запахов, табачного дыма;
- появление симптомов после приема аспирина или бета-адреноблокаторов;
- указание на наличие у пациента БА (астматический бронхит, бронхит с обструктивным компонентом) в анамнезе;
- наличие астмы/атопического заболевания у кровных родственников.
Клиническая картина БА вариабельна и зависит от фазы (обострение, ремиссия), тяжести заболевания, а также эффективности проводимого лечения. Наиболее типичное время возникновения симптомов БА – ночь или раннее утро.
К характерным клиническим симптомам БА относятся:
- свистящие хрипы в грудной клетке на выдохе, иногда слышимые на расстоянии или, напротив, только при форсированном выдохе, купируемые ингаляцией бронхолитиков или самостоятельно разрешающиеся при прекращении контакта с раздражающим фактором;
- кашель, обычно непродуктивный, реже со скудным отделяемым. БА следует заподозрить при длительном сухом кашле, особенно ночном, с пробуждением по причине кашля, а также в том случае, если кашель возникает при физической нагрузке или вдыхании холодного воздуха, если малопродуктивный кашель сопровождает или следует за респираторной вирусной инфекцией и имеет приступообразный характер, если сопутствует аллергическому риниту и/или атопическому дерматиту;
- чувство тяжести в грудной клетке;
- эпизодическая одышка (удушье), не всегда сопровождающаяся свистящими хрипами.
Наиболее типичный признак БА – приступ экспираторного удушья. Он возникает внезапно, во время него вдох происходит быстро и порывисто. За коротким и сильным вдохом следует продолжительный затрудненный активный выдох, который может сопровождаться слышными на расстоянии свистящими хрипами.
В дыхании участвуют вспомогательные мышцы пояса верхних конечностей, передней брюшной стенки. В легких на фоне ослабленного везикулярного или жесткого дыхания выслушиваются разные тембровые сухие свистящие хрипы. Нужно помнить, что при развитии астматического статуса в фазу «немого легкого» хрипы могут не выслушиваться, но в такие периоды обычно присутствуют другие признаки дыхательной недостаточности. Приступ удушья быстро проходит после применения бронхорасширяющего ингалятора или самостоятельно при прекращении контакта с раздражающим фактором. Часто после купирования приступа удушья начинает отходить вязкая слизистая скудная мокрота.
В связи с вариабельностью проявлений БА изменения со стороны дыхательной системы при физикальном обследовании могут отсутствовать, что не исключает диагноза астмы. Крепитация и хрипы на вдохе, а также односторонняя симптоматика не характерны для БА.
ИНСТРУМЕНТАЛЬНАЯ И ЛАБОРАТОРНАЯ ДИАГНОСТИКА БРОНХИАЛЬНОЙ АСТМЫ
Оценка функции внешнего дыхания при спирометрии служит важным и обязательным методом обследования взрослого пациента с подозрением на БА для подтверждения наличия и оценки степени бронхиальной обструкции.
В межприступный период при БА объем формированного выдоха за первую секунду (ОФВ1), а также пиковая скорость выдоха (ПСВ) могут быть нормальными (≥80% от должных значений).
Во время приступа, а также при недостаточном контроле заболевания обнаруживают бронхиальную обструкцию: ОФВ1 и ПСВ <80% от должных значений, индекс Генслера или модифицированный индекс Тиффно (соотношение ОФВ1/ФЖЕЛ) <70%.
Большое диагностическое значение имеет проба с бронходилататором (β2-агонистом короткого действия сальбутамолом в дозе 400 мкг). Перед применением препарата пациента необходимо обучить технике ингаляции для исключения критических ошибок, существенно снижающих доставленную дозу препарата. Бронходилатационный тест рекомендуется проводить всем пациентам с БА для определения степени обратимости обструкции и выявления скрытых обструктивных нарушений при отсутствии исходно грубых вентиляционных нарушений. Пробу оценивают через 15 мин после ингаляции бронхолитика по приросту ОФВ1:
- Абсолютный прирост ОФВ1 (мл): ΔОФВ1 = ОФВ1 после бронхолитика – ОФВ1 исходный.
- Индекс бронходилатации = ΔОФВ1 × 100%/ОФВ1 исходный.
Абсолютный прирост ОФВ1 ≥200 мл и индекс бронходилатации ≥12% от исходных показателей свидетельствуют об обратимости обструкции и характерны для БА (положительный бронходилатационный тест).
У пациентов с высокой вероятностью БА с нормальными показателями спирометрии для подтверждения диагноза рекомендуется проведение повторной спирометрии с пробой на обратимость в период наличия клинических симптомов.
Иногда, особенно в случае отрицательного бронходилатационного теста, но наличии типичных жалоб и анамнеза, пациентам с подозрением на БА рекомендуется проведение пробной терапии ингаляционными глюкокортикостероидами (ИнГКС). ИнГКС назначаются обычно в низких, средних дозах (400–800 мкг будесонида или эквипотентные дозы другого ИнГКС) в течение 6–8 нед.
В исключительных случаях возможно назначение перорального преднизолона в дозе 30 мг в сутки в течение 2 нед с дальнейшей оценкой эффекта. Улучшение или исчезновение клинических симптомов, а также улучшение функции легких (абсолютный прирост ОФВ1 ≥200 мл и индекс бронходилатации ≥12% от исходных показателей) в ответ на терапию ИнГКС расценивается как положительная проба и служит подтверждением диагноза БА.
Пикфлоуметрия – простой и доступный метод оценки ПСВ, позволяющий оценить контроль БА, ответ на терапию, гиперреактивность дыхательных путей.
Дыхательный маневр выполняется стоя или сидя минимум 2 раза в день (утром и вечером). Каждый раз регистрируется лучший показатель ПСВ после 3 попыток выполнения форсированного выдоха в пикфлоуметр с паузой, не превышающей 2 с после вдоха.
Диагноз БА можно предположить, если:
- ПСВ увеличивается более чем на 15% после ингаляции β2-агониста быстрого действия;
- ПСВ в течение суток варьирует более чем на 20% у пациента, получающего бронхолитики (и >10% у пациента, их не получающего);
- ПСВ уменьшается более чем на 15% после 6 мин непрерывного бега или другой физической нагрузки.
Вариабельность ПСВ (ΔПСВ%) вычисляют по формуле:
ΔПСВ% = (ПСВ макс – ПСВ мин) × 100%/ПСВ среднесуточное или макс.
Оксид азота (NO) в выдыхаемом воздухе служит маркером эозинофильного воспаления в дыхательных путях. Концентрация FeNO используется также для оценки эффективности противовоспалительной терапии при БА. Уровень FeNO обычно снижен у курильщиков, а также во время бронхоспазма [6, 7, 8].
Мокрота больных БА может содержать ряд характерных элементов:
- спирали Куршмана, представляющие собой штопорообразно извитые сгустки слизи (слепки бронхов), отделяющиеся по мере выхода больного из состояния приступа удушья;
- кристаллы Шарко–Лейдена, состоящие из продуктов разрушенных эозинофилов;
- эозинофилы;
- тельца Креола, представляющие скопления эпителиальных клеток бронхов;
- метахроматические клетки (тучные клетки, базофилы).
В клиническом анализе крови пациентов с БА может отмечаться эозинофилия.
Для уточнения фенотипа БА требуется проведение специфической диагностики: постановки кожных проб с аллергенами, определения уровня специфических IgE в крови (уровень общего IgE в крови не коррелирует со специфическим).
Во время развития приступа БА содержание кислорода в крови снижается в зависимости от выраженности спазма бронхов и объема захваченной им дыхательной поверхности.
При тяжелом течении БА на электрокардиограмме (ЭКГ) выявляются перегрузка и/или гипертрофия правого желудочка, нарушения проводимости по правой ножке пучка Гиса. Во время приступа астмы возможна тахикардия, которая уменьшается в межприступный период.
При БА отсутствуют специфические рентгенологические признаки, иногда обнаруживается повышенная воздушность легких (при эмфиземе).
ДИФФЕРЕНЦИАЛЬНЫЙ ДИАГНОЗ
Заболевания, с которыми врачу наиболее часто приходится проводить дифференциальную диагностику БА, представлены в таблице [3, 4].

Таким образом, для успешной диагностики заболевания необходимо выявить в клинической картине характерные черты, симптомы и признаки, не свойственным другим болезням. Комплексный подход позволит установить, что именно провоцирует проблемы с дыханием, подтвердить вариабельность бронхообструкции и на этом основании поставить правильный диагноз.
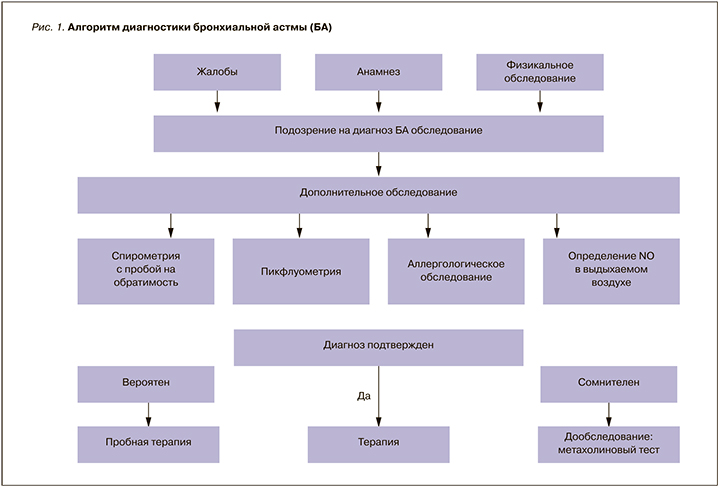
Алгоритм диагностики БА, используемый нами при оказании первичной медико-санитарной помощи в ФГБУ «Поликлиника № 1» УДП РФ, представлен на рисунке 1. Это учреждение является медицинской организацией оказания первичной медико-санитарной помощи взрослому населению г. Москвы без фиксированного территориального прикрепления и низким процентом сменяемости контингента, что позволяет экстраполировать его эпидемиологические данные на данные Москвы в целом. Особенностью организации работы ФГБУ «Поликлиника № 1» УДП РФ является расширенный штат врачей – аллергологов-иммунологов (примерно 1 штатная единица на 10 тыс. прикрепленного контингента, в то время как по Приказу Минздрава России от 07.11.2012 № 606н рекомендуется 1 штатная единица врача – аллерголога-иммунолога на 100 тыс. взрослого населения); это повышает доступность специализированной помощи и позволяет проводить аллергологическое обследование всем пациентам БА. В структуре отделения аллергологии и иммунологии, пульмонологии и инфекционных заболеваний поликлиники есть функциональный кабинет, в котором проводятся спирометрия с проведением бронходилатационных тестов при помощи портативного спирометра Micro Loop, пульсоксиметрия, определение уровня оксида азота в выдыхаемом воздухе на аппарате NObreath. Использование функциональных методов диагностики на приеме у пульмонологов и аллергологов-иммунологов позволяет провести дифференциальную диагностику респираторных симптомов, оценить степень и прогноз нарушения респираторной функции, проводить динамическое наблюдение в процессе лечения.
 Внедрение этого диагностического алгоритма позволило повысить выявляемость БА. Так, показатель распространенности заболевания (ПРЗ) БА на 1000 лиц за 5 лет наблюдения (2013–2017) в нашем учреждении вырос на 47,2%, тогда как, по данным статистики, среди взрослого населения Москвы за тот же период он снизился на 2,5% [9, 10, 11]. За 2013–2017 гг. ПРЗ БА среди взрослого населения Москвы, согласно статистике, в среднем составляет 10,54/1000, что ниже результатов нашего исследования (19,25/1000) в 1,83 раза (рис. 2).
Внедрение этого диагностического алгоритма позволило повысить выявляемость БА. Так, показатель распространенности заболевания (ПРЗ) БА на 1000 лиц за 5 лет наблюдения (2013–2017) в нашем учреждении вырос на 47,2%, тогда как, по данным статистики, среди взрослого населения Москвы за тот же период он снизился на 2,5% [9, 10, 11]. За 2013–2017 гг. ПРЗ БА среди взрослого населения Москвы, согласно статистике, в среднем составляет 10,54/1000, что ниже результатов нашего исследования (19,25/1000) в 1,83 раза (рис. 2).
Число пациентов, которым проводилось аллергообследование за годы наблюдения, увеличилось на 32,1%, что свидетельствует об увеличении направления терапевтами и врачами общей практики пациентов на обследование к врачам-аллергологам и интенсификации работы по диагностике аллергических заболеваний.
ЗАКЛЮЧЕНИЕ
Данные нашего исследования подтверждают факт снижения уровня диагностики БА и соответственно выявляемости данного заболевания в Москве. Внедрение разработанного нами алгоритма в работу врачей первичного звена будет способствовать повышению уровня диагностики БА на раннем этапе заболевания, уменьшению числа не верифицированных случаев заболевания и в целом повышению качества оказания медицинской помощи пациентам с БА на амбулаторно-поликлиническом этапе.



