Некомпактный миокард – это редкая форма врожденной кардиомиопатии, которая встречается как у взрослых, так и у детей и характеризуется чрезмерной трабекулярностью с образованием глубоких межтрабекулярных пространств. Множественные трабекулы формируют широкий некомпактный губчатый слой сердечной мышцы, в то время как слой однородного миокарда, способного к сокращению, остается тонким. Такая измененная структура сердечной мышцы приводит к быстро нарастающему ухудшению сократительной способности сердца и развитию в ряде случаев тяжелой сердечной недостаточности.
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ
Больная Л., 71 год, 31.05.2012 в 18:00 поступила в палату реанимации и интенсивной терапии терапевтического отделения № 4 Республиканской клинической больницы № 2 Минздрава Республики Татарстан – базовой клиники кафедры терапии Казанской государственной медицинской академии. Основными жалобами при поступлении были одышка в покое, усиливающаяся в горизонтальном положении, отеки нижних конечностей, периодически возникающие боли в области сердца в покое и при физической нагрузке, которые купировались изосорбида динитратом.
Анамнез: больная страдала ИБС и гипертонической болезнью около 10 лет, более 30 лет – бронхиальной астмой. В 2006 г. перенесла острый инфаркт миокарда (ОИМ), в 2009 и 2012 г. – острое нарушение мозгового кровообращения (ОНМК). Ежегодно получала стационарное лечение по поводу сердечной декомпенсации, последний раз в апреле–мае 2012 г. Выписывалась с улучшением. Дома принимала дигоксин по 0,125–0,25 мг, торасемид по 10 мг, триметазидин, изосорбида мононитрат, ацетилсалициловую кислоту (в «кардиодозах»), ипратропия бромид + фенотерол, будесонид + формотерол, преднизолон по 10 мг/сут.
Ухудшение самочувствия в виде усиления одышки было отмечено с утра дня поступления в стационар. К вечеру стало еще хуже, что стало причиной госпитализации.
Состояние больной при поступлении было тяжелым: из-за одышки она не могла лежать, наблюдались цианоз губ, отеки голеней и стоп, одышка в покое до 24 дыхательных движений в минуту. Тоны сердца были приглушены, аритмичны, частота сердечных сокращений – 122 удара в минуту, пульс – 84 в минуту, дефицит пульса – 38, артериальное давление – 150/60 мм рт.ст. Дыхание было жесткое, в нижних отделах справа ослабленное, хрипы не выслушивались. Печень не была увеличена, селезенка не пальпировалась, симптом Ф.И. Пастер-нацкого был отрицательным с обеих сторон.
Данные ЭКГ в день поступления: тахисистолическая форма мелковолновой фибрилляции предсердий со средней частотой сокращений желудочков 139 в минуту. Резкое отклонение электрической оси сердца влево. Полная блокада левой ножки пучка Гиса с преимущественной блокадой передневерхней ветви левой ножки пучка Гиса. Желудочковый комплекс типа «QS» в V1–V4. Подъем сегмента ST в V1–V6. Не исключалась гипертрофия правого желудочка (рис. 1).
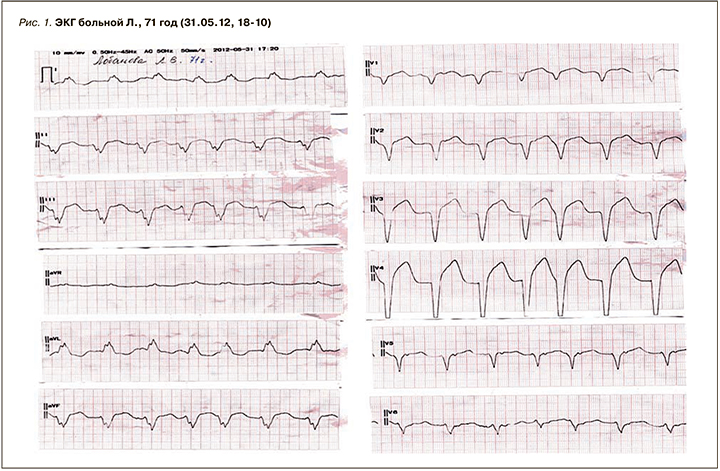
Изменений в общем анализе крови не было.
Результаты биохимического анализа крови: миоглобин – 76,8 нг/мл (N до 95); тропонин – отр.; глюкоза крови – 7,88 ммоль/л (N 3,38–5,55); Na – 134,9 ммоль/л (N 135–152); К – 3,8 ммоль/л (N 3,6–6,3); Са – 0,74 ммоль/л (N 2,2–2,75); Cl – 94 ммоль/л (N 95–110); pH – 7,28 (N 7,35–7,45); pаCO2 – 29,4 мм рт.ст. (N 35–48); pаO2 – 41,1 мм рт.ст. (N 83–108).
Коагулограмма: фибриноген общ. – 1,7 г/л (N 2–4); фибриноген Б – отр. (N отр.); тромботест III (N IV–V); МНО – 1,05 ед. (N 0,98–1,3).
На фоне терапии дигоксином, фуросемидом, спиронолактоном, гепарином, дофамином, реополиглюкином состояние больной прогрессивно ухудшалось: усиливалась одышка (ЧДД 32 в минуту), снижалось АД до 60/40 мм рт.ст., на ЭКГ наблюдалась картина резкой перегрузки правых отделов сердца.
01.06.2012 в 05:30 больная скончалась.
Клинический диагноз «ишемическая кардиомиопатия. Постоянная форма мерцательной аритмии. Полная блокада левой ножки пучка Гиса с преимущественной блокадой ПВВЛНПГ. Гипертоническая болезнь III стадии, 4 группы риска с поражением сердца (ИБС, постинфарктный кардиосклероз, ОИМ в 2006 г.), сосудов головного мозга (ОНМК в 2006, 2012 г.)».
Хроническая сердечная недостаточность (ХСН) IIБ, функциональный класс 4. ХОБЛ, тяжелое течение, дыхательная недостаточность 3 ст. Осложнения заключительного диагноза: гидроперикард. Асцит. Легочное сердце. Тромбоз ветвей легочной артерии? Острая сердечно-легочная недостаточность. Сопутствующий диагноз: сахарный диабет 2 типа, субкомпенсация.
Патологоанатомический диагноз. Основной:
1. Хроническая ИБС, диффузный и периваскулярный кардиосклероз, стенозирующий коронаросклероз 3 ст., 3 стадии. Ишемическая кардиомио-патия (интрамуральной зоны левого желудочка сердца). Хроническая аневризма левого желудочка сердца, аневризма восходящей дуги аорты с дилатацией просвета, аневризма грудного и брюшного отделов аорты с тромботическими массами. Решетчатый миокард правого и левого желудочков сердца (гипертрофия трабекулярных и сосочковых мышц сердца с тромбообразованием в межмышечных пространствах).
2. Гипертоническая болезнь с преимущественным поражением сердца, гипертрофия миокарда ЛЖ – 1,7 см, ПЖ – 0,6 см, МС – 540 гр.
Осложнения: ХСН, правосторонний гидроторакс. Общее венозное полнокровие с застойной индурацией селезенки, почек, мускатная печень, застойный тромб в просвете правого желудочка, тромбоз легочного ствола и мелких сосудов микроциркуляторного русла легких. Эмфизема легких с гемосидерозом, пневмосклероз, перибронхиальный склероз.
Сопутствующие: атеросклероз аорты 3–4 ст. Сахарный диабет на фоне очагового склероза и липоматоза ткани поджелудочной железы. Хронический геморрагический эзофагит.
Эпикриз: причиной смерти больной Л., 71 года, явился тромбоз в легочном стволе и сосудах микроциркуляторного русла легких, развившийся как осложнение ХСН (рис. 2 и 3).

Таким образом, у нашей пациентки был выявлен «губчатый миокард» (некомпактный миокард – spongy myocardium, noncompaction myocardium).
НЕКОМПАКТНЫЙ МИОКАРД: ЭПИДЕМИОЛОГИЯ, КЛАССИФИКАЦИЯ И КЛИНИКА
В мировой научной литературе первое сообщение о некомпактном миокарде (НМ) появилось в 1986 г., в нашей стране заболевание впервые было описано в 1998 г. По данным различных авторов, распространенность НМ варьирует от 0,05 до 0,24%. Некомпактность левого желудочка (ЛЖ) может иметь место у людей различных возрастных групп – от 1 месяца до 71 года, но преимущественно встречается у лиц молодого возраста. Это может быть связано с тем, что большинство пациентов с развернутой клинической картиной заболевания умирает, не дожив до среднего возраста или даже до совершеннолетия.
В связи со сложностью диагностики и недостаточной осведомленностью врачей об этом заболевании синдром НМ часто остается нераспознанным. Возможно, эта патология встречается значительно чаще, чем диагностируется. Описаны две формы данного заболевания – изолированная и неизолированная, ассоциированная с такими врожденными заболеваниями, как:
- врожденный порок сердца – дефект межпредсердной и межжелудочковой перегородки (МЖП), стеноз легочной артерии;
- нейромышечная патология – метаболическая миопатия, синдром Barth, синдром Ohtahara, синдром Roifmana, синдром Melnick–Needles, синдром Noonan, мышечная дистрофия Becker, мышечная дистрофия Emery–Dreifus, миотубулярная кардиомиопатия;
- дефекты лицевого черепа – выступающий лоб, двустороннее косоглазие, микрогнатия, расщепленное нёбо или волчья пасть.
НМ чаще формируется в ЛЖ. У части больных в процесс вовлекается и правый желудочек (ПЖ), некоторые авторы говорят о поражении обоих желудочков у 40% больных. Вопрос об изменении ПЖ до сих пор остается дискутабельным, так как нормальный вариант повышенной трабекулярности ПЖ очень трудно отличить от патологического некомпактного миокарда. Впервые НМЛЖ внесен в классификацию кардиомиопатий экспертами ВОЗ в 1995 г. как неклассифицируемая кардиомиопатия (КМП). По современным представлениям, некомпактность сердечной мышцы является результатом нарушения эмбриогенеза на ранних стадиях развития зародыша, когда сердце состоит из неплотной сеточки трубчатых мышечных волокон (губчатый миокард), которые в процессе развития сердечной мышцы постепенно «срастаются». Во внутриутробном периоде, когда венозное кровообращение развито еще недостаточно, выстланные эндокардом трабекулы участвуют в осуществлении питания сердечной мышцы. При нормальном развитии большие пространства с сеткой балочек – трабекул уменьшаются, уплощаются и срастаются, что приводит к выравниванию поверхности эндокарда ЛЖ. Если процесс развития нарушается, остается сообщение между полостью ЛЖ и пустотами между трабекулами – балками, к которым поступает кровь из полости ЛЖ. Причины нарушения уплотнения миокарда ЛЖ при НМЛЖ до конца не выяснены. Считают, что перегрузка давлением или ишемия миокарда способствуют предотвращению регресса эмбриональных миокардиальных синусоид, вследствие чего образуется постоянная связь между глубокими межтрабекулярными пространствами не только с полостью ЛЖ, но и с коронарными сосудами. Это и составляет основу изолированной некомпактности миокарда.
В клинической картине наиболее часто встречается триада: сердечная недостаточность (73%), желудочковые и наджелудочковые нарушения ритма (41%) и тромбоэмболические осложнения (33%).
Клинические аспекты НМЛЖ не являются специфичными для данной КМП. Заболевание длительное время может протекать бессимптомно. НМЛЖ впервые выявляется при рутинных исследованиях как «случайная находка». Однако чаще всего основным клиническим проявлением данной патологии является прогрессирующая сердечная недостаточность. Для больных НМЛЖ характерно нарушение систолической и диастолической функции ЛЖ. Считается, что одним из возможных механизмов возникновения систолической дисфункции является хроническая ишемия миокарда, обусловленная нарушением коронарной микроциркуляции. Диастолическая дисфункция ЛЖ обусловлена нарушением процессов расслабления и заполнения в результате наличия патологической трабекулярности ЛЖ.
ДИАГНОСТИКА НЕКОМПАКТНОГО МИОКАРДА
Отличить НМ от других причин сердечной недостаточности сложно, дифференциальный диагноз должен проводиться с дилатационной кардиомио-патией (ДКМП), гипертрофической кардиомиопатией (ГКМП), гипертоническим сердцем, тромбозом ЛЖ, добавочными трабекулами, ложными хордами, персистирующими синусоидами при аномальном отхождении левой коронарной артерии от легочного ствола, атрезией легочного ствола, атрезией легочной артерии с интактной МЖП.
Различные нарушения ритма и проводимости встречаются практически у всех больных с НМЛЖ. Среди них первое место по частоте занимают желудочковые аритмии. Фибрилляция предсердий отмечается у 25% больных, пароксизмальная или постоянная форма желудочковой тахикардии – у 47%. Среди больных с НМЛЖ у 88–94% выявляются изменения ЭКГ. Они многообразны и малоспецифичны. Для больных с НМЛЖ характерны следующие изменения на ЭКГ: отклонение электрической оси сердца влево, признаки гипертрофии миокарда ЛЖ, атриовентрикулярная блокада разной степени, блокада левой ножки пучка Гиса, синдром Вольфа–Паркинсона–Уайта (преимущественно В-тип), фибрилляция предсердий и другие аритмии.
Кроме явлений застойной сердечной недостаточности и нарушений ритма, клиническими проявлениями НМ могут быть тромбоэмболические осложнения. Причиной системных и легочных эмболий при НМЛЖ чаще всего служит фибрилляция предсердий с последующим формированием тромбоза в области межтрабекулярных пространств, где скорость кровотока значительно снижена.
Основным методом диагностики НМЛЖ служит УЗИ сердца (двумерное трансторакальное, при необходимости чреспищеводное, с контрастированием). Систематизированные эхокардиографические критерии диагностики НМЛЖ предложены Jenni R. и Oechslin Е. К ним относят:
- утолщение стенки ЛЖ за счет чрезмерно выдающихся в полость желудочка трабекул с глубокими межтрабекулярными синусами, составляющими некомпактный слой. Этот слой измеряется в месте наибольшей толщины в конце систолы, причем соотношение некомпактного слоя к «плотному» истинному миокардиальному слою должно быть больше 2;
- визуализацию при цветном допплеровском картировании глубоких межтрабекулярных синусов, соединяющихся с полостью ЛЖ с множественными турбулентными потоками крови в них;
- наличие множественных аномальных трабекул (хорд) в полости ЛЖ, определяющихся преимущественно из 4-камерной позиции;
- отсутствие другой органической патологии структур сердца и сосудов (в случае изолированного синдрома).
 Обычно «некомпактность» поражает верхушечные и средние сегменты ЛЖ. Нарушения сократимости могут касаться не только сегментов с явными чертами некомпактности, но и миокарда всего желудочка, что приводит к снижению глобальной сократительной функции сердца. В литературе описаны случаи фракции выброса ЛЖ в пределах 12–38%, однако в 12–20% случаев общая сократительная способность длительное время сохранялась.
Обычно «некомпактность» поражает верхушечные и средние сегменты ЛЖ. Нарушения сократимости могут касаться не только сегментов с явными чертами некомпактности, но и миокарда всего желудочка, что приводит к снижению глобальной сократительной функции сердца. В литературе описаны случаи фракции выброса ЛЖ в пределах 12–38%, однако в 12–20% случаев общая сократительная способность длительное время сохранялась.
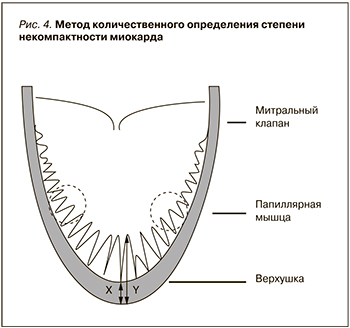
С. Lilje et al. в 2006 г. предложили метод количественного определения степени некомпактности миокарда по соотношению слоя «плотного» истинного миокарда (Х) к толщине всей стенки сердца на уровне верхушки ЛЖ (Y) (рис. 4). Величину соотношения 0,33–0,26 было решено расценивать как «мягкую» некомпактность, 0,25–0,2 – как умеренную, меньше 0,2 – как тяжелую. Данная величина была введена как прогностический признак дальнейшего развития заболевания и возникновения осложнений, поскольку тесно коррелировала со степенью и скоростью развития сердечной недостаточности.
В отдельных случаях облегчить диагностику могут магнито-резонансное исследование и компьютерная томография. Они могут быть рекомендованы как дополнительные методы. Из других визуализационных методик, применяемых для диагностики НМ, нужно отметить катетеризацию камер сердца, контрастную вентрикулографию, суточное холтеровское мониторирование, электрофизиологическое исследование при тяжелых нарушениях ритма для решения вопроса о необходимости имплантации кардиовертера-дефибриллятора, генетическое исследование.
Этиотропное лечение НМ неизвестно. Возможно и необходимо лечить недостаточность кровообращения и нарушения ритма сердца в соответствии с рекомендациями по лечению и профилактике этих синдромов и профилактике тромбоэмболических осложнений. Всем больным с доказанным НМ, независимо от размера и степени дисфункции ЛЖ, показаны оральные антикоагулянты. В работе М. Toyono et al. показано, что применение β-адреноблокатора карведилола улучшает диастолическую и систолическую функцию ЛЖ, уменьшает степень гипертрофии и выраженность трабекуляризации у больных НМ, что улучшает их прогноз и качество жизни.
У пациентов с различными видами аритмий, которые могут быть причиной внезапной смерти и эмболических осложнений, необходимо ежегодное проведение суточного мониторирования ЭКГ, назначение антиаритмической терапии, имплантация кардиовертера-дефибриллятора. Трансплантация сердца показана больным с НМЛЖ при прогрессирующей, рефрактерной к лечению СН.
Прогноз больных с НМЛЖ зависит от пораженных сегментов, общей сократительной способности миокарда, времени возникновения и скорости нарастания симптомов СН. По данным I. Jedlinsky et al., смертность в течение 6 лет составила 50%, а по данным E. Oechslin et al., около 80%. Особенно негативный прогноз наблюдали у пациентов с фракцией выброса менее 35%.
У 44% лиц с НМ наблюдают передающиеся из поколения в поколение проявления этой патологии, что свидетельствует о ее наследственном характере. Учитывая это, обязательно обследование ближайших родственников, поэтому мы обследовали 44-летнюю дочь и внуков 17 и 8 лет умершей пациентки.
Дочь и внучка оказались здоровы: при эхокардиографии (ЭхоКГ) наблюдался вариант нормы. У внука 8 лет жалоб не было, при ЭхоКГ были выявлены три дополнительные трабекулы в области верхушки ЛЖ и одна в полости ПЖ. Камеры сердца не расширены. Фракция выброса равна 65%. В норме массивные мышечные трабекулы могут встречаться в ПЖ, при этом наличие их в ЛЖ (более трех) считается патологией. Заключение: необходимо наблюдение за внуком.
Что касается родителей умершей больной, то ее мать скончалась в возрасте 86 лет от заболевания головного мозга, а отец в 60 лет от ОИМ.
ЗАКЛЮЧЕНИЕ
Таким образом, НМ является редкой врожденной кардиомиопатией. До сих пор до конца не изучены все генетические аспекты этого заболевания. Симптомы НМ неспецифичны и иногда проявляются только с возрастом, в связи с чем его редко диагностируют и часто неадекватно проводят лечение. В то же время неблагоприятный прогноз и высокая летальность при синдроме НМ определяют необходимость его распознавания на ранних стадиях и дифференцированного подхода к лечению в зависимости от тяжести состояния больного с использованием современных методов как консервативного, так и хирургического лечения.
«Золотым стандартом» в диагностике НМ служит ЭхоКГ.



